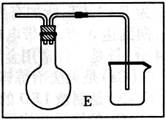
(6分)按图中所示装置,用两种不同操作分别进行实验.回答有关问题:
(1)按图示连接好装置,打开止水夹a,在B中可观察到的现象是 ,
A中发生反应的化学方程式是 ;
(2)反应片刻后,夹紧止水夹a,此时可观察到的现象有:__ __,B中发生反应的离子方程式是: 。
菠菜营养丰富,在营养价值上是一种高效的补铁剂。但因草酸含量高,因而吃起来有涩味。某学校化学兴趣小组的同学拟通过实验探究以下问题:
①菠菜是否含有丰富的铁;
②菠菜中草酸及草酸盐的含量(以C2O42-计);
通过上网查询,获得以下资料:草酸又名乙二酸,其酸性比乙酸稍强,草酸及其盐具有较强的还原性,其中草酸钙不溶于水。
他们设计的实验步骤如下:
Ⅰ.取菠菜样品,按如下步骤进行实验,观察实验现象。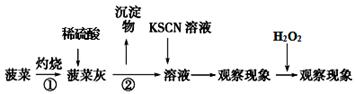
Ⅱ.另取一份菠菜样品研磨成汁后,在少量开水中煮沸2~3 min,冷却后过滤得滤液。向滤液中加入足量Ca(OH)2溶液,然后再加入足量试剂X,观察现象。并过滤得CaC2O4固体。
Ⅲ.用稀HCl溶解CaC2O4,并加水配制成100mL溶液.每次准确移取25.00mL该溶液,用0.0100mol•L-1KMnO4标准溶液滴定,平均消耗标准溶液VmL。(不考虑Cl-被KMnO4氧化。)
请回答以下问题:
(1)操作①中使用的仪器除三脚架、泥三角、酒精灯、玻璃棒外,还需要的硅酸盐质仪器 ,操作②的名称是 。
(2)通过资料分析,菠菜中的Fe是+2价还是+3价? 。
步骤I中 (填现象)可以证明该结论?
(3)通过步骤Ⅱ可以确定菠菜中含有草酸类物质。由于滤液中含有CO32-,故需加入试剂X排除CO32-的干扰。
则X是 (写化学式),加入试剂X后可观察到沉淀部分溶解。
(4)步骤Ⅲ中用到的玻璃仪器除烧杯、锥形瓶、胶头滴管、玻璃棒外,还有 ,该步骤中滴定操作的终点如何判断________________;所涉及的离子反应方程式 。
(5)若样品的质量为W g,则菠菜中草酸及草酸盐(以C2O42-计)的质量分数为___ __。
NiSO4·6H2O是一种绿色易溶于水的晶体,广泛用于镀镍、电池等,可由电镀废渣(除镍外,还含有铜、锌、铁等元素)为原料获得。操作步骤如下: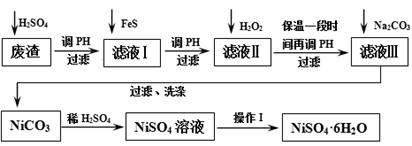
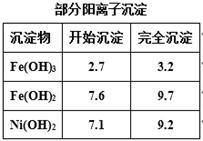
回答下列问题:
(1)向滤液Ⅰ中加入FeS是为了除去Cu2+、Zn2+等杂质,除去Cu2+的离子方程式为_______ 。
(2)常温下,用H2O2充分氧化Fe2+后,再调pH=4,目的是____ ___。
此时溶液中c(Fe3+)= ________ 。(已知25℃时,Fe(OH)3的Ksp= 2.64×10—39)。
(3)H2O2也可用NaClO3代替,写出在酸性条件下用氯酸钠氧化Fe2+的离子方程式为: 。
(4)滤液Ⅲ溶质的主要成分是NiSO4,加Na2CO3过滤后,再加适量稀硫酸溶解又生成NiSO4,
这两步操作的 ______。
(5)操作Ⅰ的步骤是:调pH为2~3,蒸发浓缩,冷却结晶,过滤,用少量乙醇洗涤并晾干。
则“调pH为2~3”的目的是_________ ______。
(6)产品晶体中有时会混有少量的绿矾FeSO4· 7H2O 其原因可能是___ ______。
硫酸亚铁是一种重要的工业原料,实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备绿矾(FeSO4·7H2O)晶体,工艺流程如下所示:
(1)将过程③中的产生的气体通入下列溶液中,溶液不会褪色的是__________;
| A.品红溶液 | B.红色的酚酞试液 |
| C.酸性KMnO4溶液 | D.紫色石蕊溶液 |
(2)Z是_____,此时溶液X中发生反应的离子方程式为_____________________________。
(3)检验溶液Y中含有金属阳离子的实验方法是______________________。
(4)操作Ⅲ、Ⅳ等实验操作步骤为蒸发、冷却结晶、 (填操作名称)、洗涤。
如下图所示,蒸发操作中的一处错误是 。
(5)测定绿矾产品中Fe2+含量的实验步骤:
a.称取6.0产品,溶解,在250mL容量瓶中定容;
b.量取25mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01mol•L-1KMnO4溶液滴定至终点,消耗KMnO4溶液体积为40mL(滴定时发生反应的离子方程式为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O)。
①计算上述产品中FeSO4•7H2O的质量分数为________;
②若用上述方法测定的产品中FeSO4•7H2O的质量分数偏低(测定过程中产生的误差可忽略),其可能原因有___________(只回答一条即可)。
(15分)肼是重要的化工原料。某探究小组利用下列反应制取水合肼(N2H4·H20)。
CO(NH2)+2NaOH+NaCl0=Na2C03+N2H4·H20+NaCI
实验一:制备NaClO溶液。(实验装置如图所示).
(1)配制30%NaOH溶液时,所需玻璃仪器除量筒外,还有_______________(填标号)。
A.容量瓶B.烧杯C.烧瓶 D.玻璃棒
(2)锥形瓶中发生反应的化学方程式是_________________________。
(3)因后续实验需要,需利用中和滴定原理测定反应后锥形瓶中混合溶液的NaOH的浓度。请选用所提供的试剂,设计实验方案。提供的试剂:H202溶液、FeCl2溶液、0.1000mol·L-1盐酸、甲基橙试液
_________________________________________.
实验二:制取水合肼。(实验装置如图所示)
控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应。
加热蒸馏三颈烧瓶内的溶液,收集108~114℃馏分。
(己知:N2H4·H20+2NaClO=N2↑+3H20+2NaCl)
(4)分液漏斗中的溶液是_____________________(填标号)。
A.CO(NH2)2溶液
B.NaOH和NaClO混合溶液
选择的理由是____________________________________________。
实验三:测定馏分中肼含量。
称取馏分5.000g,加入适量NaHC03固体,加水配成250 mL溶液,移出25.00 mL,用0.1000mol·L-1的I2溶液滴定。滴定过程中,溶液的pH保持在6.5左右。
(己知:N2H4·H20+2I2=N2↑+4HI+H20)
(5)滴定过程中,NaHC03能控制溶液的pH在6.5左右,原因是_____________________。
(6)实验测得消耗I2溶液的平均值为1 6.00mL,馏分中水合肼(N2H4·H20)的质量分数为______________。
氢化锂(LiH)在干燥的空气中能稳定存在,遇水或酸能够引起燃烧。某活动小组准备使用下列装置制备LiH固体。
甲同学的实验方案如下:
(1)仪器的组装连接:上述仪器装置接口的连接顺序为_________________,加入药品前首先要进行的实验操作是_______________(不必写出具体的操作方法);其中装置B的作用是_____________________。
(2)添加药品:用镊子从试剂瓶中取出一定量金属锂(固体石蜡密封),然后在甲苯中浸洗数次,该操作的目的是________________________________________,然后快速把锂放入到石英管中。
(3)通入一段时间氢气后加热石英管,在加热D处的石英管之前,必须进行的实验操作是
______________________________________________________________________。
(4)加热一段时间后停止加热,继续通氢气冷却,然后取出LiH,装入氮封的瓶里,保存于暗处。采取上述操作的目的是为了避免LiH与空气中的水蒸气接触而发生危险。(反应方程式:LiH + H2O =" LiOH" + H2↑),分析该反应原理,完成LiH与无水乙醇反应的化学方程式_____________________。
(5)准确称量制得的产品0.174g,在一定条件下与足量水反应后,共收集到气体470.4 mL(已换算成标准状况),则产品中LiH与Li的物质的量之比为____________________。
(6)乙同学对甲的实验方案提出质疑,他认为未反应的H2不能直接排放,所以在最后连接了装置E用来收集H2,请将E装置补充完整。