某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动。
【提出问题】这种淡黄色粉末是什么?有什么性质和用途?
【查阅资料】①硫是淡黄色粉末,不溶于水;
②过氧化钠(Na2O2)是淡黄色粉末,溶于水并能与水反应,“载人宇宙飞船或潜水艇中一般都要安装盛放过氧化钠(Na2O2)颗粒的装置”
【猜想与探究】
猜想:淡黄色粉末可能是:a.硫;b.过氧化钠;c.硫和过氧化钠的混合物
【实验与结论】
| |
实验操作 |
实验现象 |
实验结论 |
| 猜想 |
在一支洁净的试管中加入适量的上述淡黄色粉末,再加入足量的蒸馏水,充分振荡 |
|
猜想a、c不成立,猜想b成立。 |
【提出问题】过氧化钠是否为一种制氧剂?与人呼出的哪种气体发生反应?
【提出猜想】过氧化钠与人呼出的N2或CO2或水蒸气反应并生成氧气。
【进行实验】
实验Ⅰ:验证过氧化钠与氮气反应并生成氧气。
王轩同学设计如下图所示装置:
(1)实验现象及结论:观察到____________现象,判断过氧化钠与氮气没有发生反应。
实验Ⅱ:验证过氧化钠与水蒸气反应并生成氧气。
华宇同学设计了如下图所示装置
(2)其中A装置的作用是____________。
(3)实验现象及结论:带火星的木条复燃。
实验Ⅲ:验证过氧化钠与二氧化碳反应并生成氧气。李杰在老师的指导下也设计了如下图所示装置。(不考虑稀盐酸的挥发)
| 实验操作 |
主要实验现象 |
实验结论及解释 |
|
| ① |
检查装置的气密性。 向装置中加入药品。 |
|
装置的气密性良好。 |
| ② |
打开分液漏斗活塞,向A装置中缓慢加入稀盐酸。 |
A装置中观察到的现象有__________, C装置中有气泡出现。 |
A装置中发生反应的化学方程式为________; |
| ③ |
一段时间后用带火星的木条在D内进行检验。 |
带火星的木条复燃。 |
过氧化钠与二氧化碳反应并生成氧气。 |
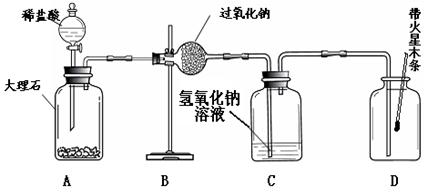
(4)实验记录
【实验反思】
张红同学对实验Ⅲ的设计提出疑问:该实验不能证明二氧化碳与过氧化钠确实发生了反应,你认为他的理由是_____ ___。请你回答如何改进该实验 。
长途运输鱼苗时,常在水中加入少量过氧化钙(CaO2)固体。甲、乙两位同学发现往水中投入过氧化钙时产生气泡。
【提出问题】当把过氧化钙投入足量水中时,最终生成什么物质?
【进行猜想】甲同学:生成氧化钙和氧气;乙同学:生成氢氧化钙和氧气。
你赞同的猜想是(填“甲”或“乙”),其理由是;
【实验探究】
(1)打开右图装置中分液漏斗的活塞,控制滴加水速度,观察到
试管内有气泡产生。
①(填实验操作),
说明生成的气体是氧气。
②实验过程中,发现烧杯中有气泡出现,该现象说明。
(2)请设计一个实验方案来验证乙同学猜想的生成物中有“氢氧化钙”:
| 实验步骤及操作方法 |
预期的实验现象 |
结论 |
| ①取少量过氧化钙放入试管中,加足量水,振荡, ②。 |
①产生气泡, ②。 |
过氧化钙和水反应产生的另一种物质是氢氧化钙 |
【问题讨论】
(1)运输鱼苗时,在水中加入少量过氧化钙的主要目的是;
(2)过氧化钙和水反应的化学方程式为。
实验室利用下列装置可以制取某些气体,请据图回答问题:
(1)这五个装置示意图中,有一个装置是错误的,指出错误装置是(填序号)。
(2)图示中仪器①的作用;实验室用高锰酸钾来制取氧气,可选择A作发生装置,但要对A进行改进,改进的方法是;实验室若用B作发生装置制氧气,则该反应方程式为。
(3)常温下,硫化氢(H2S)是一种有臭鸡蛋气味的气体,实验室可用硫化亚铁(FeS)固体和稀硫酸反应制得,该反应方程式为FeS + H2SO4(稀)= H2S↑+Fe SO4,则应选择
(填序号,下同)来作发生装置。
(4)NO气体难溶于水,密度略大于空气,易与氧气反应生成NO2,则应选择装置来收集NO。
如右图所示:水槽内盛有澄清石灰水,点燃高低两支蜡烛,用钟罩将其扣在水槽内。一段时间后可以观察到的现象有:①钟罩内澄清的石灰水变浑浊;②;③。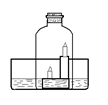
现象①用化学方程式可表示为;现象②和③出现的原因是、。
④某同学用上述实验来测定空气中氧气的体积含量,结果发现与理论数据有偏差,其原因可能是。(提示:本装置气密性良好)
根据下列装置图.回答有关问题:
(1)写出装置中标号仪器的名称:①;②。
(2)实验室用高锰酸钾制取氧气,可选用的发生装置是(填字母)。
(3)写出实验室制取二氧化碳的化学方程式,该反应
属于反应(填基本反应类型)根据上图组装一套制取干燥CO2的装置
(用字母表示),验满的方法是。
请根据下图所示实验,回答问题。
甲乙丙
(1)甲中可观察到硫在氧气中燃烧,发出 火焰;
(2)乙中仪器a的名称是 ,玻璃管中的现象是 ,该装置的不足之处是 ,玻璃管中反应的化学方程式是。
(3)丙中铜片上的现象是 ,由此得出可燃物燃烧的条件是 。