下表是氯化铵在不同温度下的溶解度:
| 温度(℃) |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
| 溶解度(g/100g水) |
29.4 |
33.3 |
37.2 |
41.4 |
45.8 |
50.4 |
55.0 |
60.2 |
(1)从表中可知:随温度升高氯化铵的溶解度 。
(2)60℃时,向盛有50 g水的烧杯中加入30 g氯化铵,充分搅拌,可得到氯化铵的 (填“饱和”或“不饱和”)溶液,溶质的质量分数是 。
(3)A烧杯是70℃时,溶剂为100g的氯化铵不饱和溶液,经过如下图的变化过程(在整个过程中不考虑水分的蒸发)。
Ⅰ. C烧杯溶液中溶质的质量为 g。
Ⅱ.70℃时,将A烧杯中的溶液恒温蒸发10 g溶剂后,析出a g固体,再继续恒温蒸发30g溶剂,则析出固体b克,则b克 3a 克(填“<、≤、>、≥或=”)。
Ⅲ.有关三个烧杯中溶液的说法,错误的是 (填字母序号)。
a.B烧杯中溶液是不饱和溶液
b.A、B、C烧杯中的溶液在变化过程中,溶解度一定改变
c.由60℃降温至50℃时溶液质量一定减少
d.降温至60℃时,溶液中溶质质量分数一定不变
e.降温至30℃,烧杯中一定有NH4Cl晶体析出
(10分)净水丸能对饮用水进行快速杀苗消毒,倍受人们青眯。药丸分内外两层.使用时,直接将它投入适量的水中,外层的优氯净(C303N3Cl2Na)先与水反应,生成的次氯酸(HClO)起杀菌消毒作用;几分钟后.内层的亚硫酸钠(Na2S03)将水中的余氯(次氯酸等)除去。回答下列问题:
(1) C303N3Cl2Na由种元素组成。
(2)HCl0中氧元素的化合价为。
(3)净化水除了上述方法外.请你另举一例:。
(4)除去余氯的反应之一为:Na2S03+HClO=Na2S04+X,X的化学式为。
(5)使用净水丸时.能否先破碎后使用?(填”能”或“不能”)。
联合国将2011年定为"国际化学年",以纪念化学取得的成就以及对人类文明的贡献.也适逢居里夫人因发现镭元素获得诺贝尔化学奖l00周年。已知镭原子的核内质子数为88。常温下,镭是一种银白色同体.质软,密度为6.0
,熔点为700℃,易与水反应生成氢氧化镭(镭显+2价)和氢气。
回答下列问题:
(1)镭原子的核外电子数为。
(2)从上述叙述中找出镭的一点物理性质:。
(3)写出镭(
)与水反应的化学方程式:。
(4)举出一个例子,说明化学对人类作出的贡献:。
现在,很多家庭自备有干粉灭火器,它是利用压缩的二氧化碳吹干粉(主要含有磷酸二氢铵)来灭火。灭火器的罐体有铝合金和铁质的,前者的使用年限约是后者的6倍。回答下列问题:
(1)二氧化碳可利用空气中最多的气体来代替,该气体是。
(2)磷酸二氢铵(
)溶于水时与
相似,会出现明显的(填"升温"或"降温")现象。
(3)
在灭火时的作用之一是:它受热分解后在可燃物表面形成一层玻璃状的覆盖层.其灭火原理是。
(4)为了变废为宝,报废灭火器中的
可作为(填写字母标号)使用。
| A. | 氮肥 | B. | 磷肥 | C. | 钾肥 | D. | 复合肥料 |
(5)用化学知识解释.两种罐体的使用年限为什么不同?。
科学家最近发明了一种家用机器,它能吃进塑料吐出燃料(原油)。
(1)塑料属于(填"天然"或"合成")材料。
(2)这一发明有助于解决的环境污染问题是。
(3)原油属于(填"纯净物"或"混合物")。
(4)原油经过蒸馏可分离出汽油、煤油、等燃料,此过程发生(填"物理"或"化学")变化。
(9分)实验室常用下列仪器装置制备或收集气体: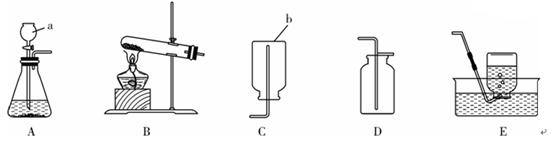
(1)写出图中标号仪器的名称:
,
。
(2)实验室制备
时,应选用的气体发生装置是(填字母,下同),收集装置是,制备
气体的反应原理是(用化学反应方程式表示):,该反应基本类型是。
(3)实验室用反应
制取氧气时,应选用的气体发生装置是,收集装置是,其中
起作用。