已知:
| 药品名称 |
熔点/℃ |
沸点(℃) |
密度g/cm3 |
溶解性 |
| 正丁醇 |
-89.5 |
117.7 |
0.8098 |
微溶于水、溶于浓硫酸 |
| 1-溴丁烷 |
-112.4 |
101.6 |
1.2760 |
不溶于水和浓硫酸 |
根据题意完成下列填空:
(一)制备1-溴丁烷粗产品在如图装置的圆底烧瓶中依次加入NaBr,10 mL 正丁醇,2粒沸石,分批加入1:1的硫酸溶液,摇匀,加热30 min。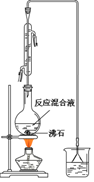
(1)写出制备1-溴丁烷的化学反应方程式:__________________________________________________
(2)反应装置中加入沸石的目的是__________________。配制体积比为1:1的硫酸所用的定量仪器为 (选填编号)。
a.天平 b.量筒 c.容量瓶 d.滴定管
(3)反应装置中,除了产物和水之外,还可能存在 、 等有机副产物。
(4)若用浓硫酸进行实验,有机层中会呈现棕黄色,除去其中杂质的正确方法是 (选填编号)。
a.蒸馏 b.氢氧化钠溶液洗涤
c.用四氯化碳萃取 d.用亚硫酸钠溶液洗涤
(二)制备精品
将得到的粗1-溴丁烷依次用浓硫酸、水、10% 碳酸钠、水洗涤后加入无水氯化钙进行干燥,然后再将1-溴丁烷按图装置蒸馏。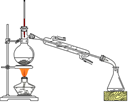
(5)收集产品时,控制的温度应在_________℃左右;区分1-溴丁烷精品和粗品的一种方法是____________________。
(6)实验制得的1-溴丁烷的质量为10.895 g,则正丁醇的转化率为 。(保留3位小数)。
正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛。
发生的反应如下:
反应物和产物的相关数据如下:
| 沸点/℃ |
密度(g.cm-3) |
水中溶解性 |
|
| 正丁醇 |
117.2 |
0.8109 |
微溶 |
| 正丁醛 |
75.5 |
0.8107 |
微溶 |
实验步骤如下:
①将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中。
②在A中加入4.0g正丁醇和几粒沸石,加热。当有蒸汽出现时,开始滴加B中溶液。滴加过程中保持反应温度为90~95℃,在E中收集90℃以下的馏分。
③将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77℃馏分,产量2.0g。
回答下列问题:
(1)B仪器的名称是 ,D仪器的名称是 。
(2)沸石的作用是 。
(3)将正丁醛粗产品置于分液漏斗中分液时,水在 层(填“上”或“下” )
(4)反应温度应保持在90~95℃,其原因是 。
(5)本实验中,正丁醛的产率为 %。
实验室配制500mL0.2mol•L﹣1的FeSO4溶液,具体操作步骤为:
①在天平上称取一定质量的绿矾(FeSO4•7H2O),把它放在烧杯中,用适量的蒸馏水使其完全溶解;
②把制得的溶液小心的注入500mL的容量瓶中;
③继续向容量瓶中滴加蒸馏水至液面距刻度线1~2cm处时,改用胶头滴管小心滴加,直到溶液的凹液面恰好与刻度线相切为止;
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次的洗涤液都转入容量瓶中,并轻轻摇匀;
⑤将容量瓶塞好,充分摇匀。
请填写下列空白.
(1)用托盘天平称取的绿矾的质量为: ;
(2)上述操作的正确顺序为: ;
(3)本次实验过程中多次用到玻璃棒,在溶解时玻璃棒的作用是: ,在移液时玻璃棒的作用是: .
(4)观察液面时,若俯视刻度线,会使所配制的溶液的浓度 (填“偏高”、“偏低”或“无影响”下同);加蒸馏水时不慎超过了刻度线后倒出部分溶液,使液面与刻度线相切,会 ;
(5)用ρ=1.84g•mL﹣1,质量分数为98%的浓硫酸配制200mL1mol•L﹣1的稀硫酸与上述配制溶液的步骤上的差别主要有三点:
①计算:理论上应取浓硫酸的体积V= mL(精确到小数点后两位);
②量取:由于量筒是一种粗略的量具,如想精确量取,必需选用 (填仪器名称).
③溶解:稀释浓硫酸的方法 .
明矾石是制取钾肥和氢氧化铝的重要原料,明矾石的组成和明矾相似,此外还含有氧化铝和少量氧化铁杂质。具体实验步骤如下图所示: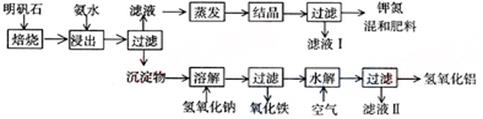
根据上述图示,完成下列填空:
(1)明矾石焙烧后用稀氨水浸出。配制500mL稀氨水(每升含有39.0g氨)需要取浓氨水(每升含有250.0g氨) mL。( 精确到小数点后一位)
(2)氨水浸出后得到固体混合体系,过滤,滤液中除K+、NH4+外,还有大量的SO42-。检验SO42-的方法是 。
(3)写出沉淀物中所有物质的化学式 。
(4)滤液I的成分是水和 。
(5)为测定混合肥料K2SO4、(NH4)2SO4中钾的含量,请完善下列步骤:
①称取钾氮肥试样并溶于水,加入足量 溶液,产生白色沉淀。
② 、洗涤、 ,(依次填写实验操作名称)。
③冷却、称重。
(6)若试样为mg,沉淀的物质的量为nmol,则试样中K2SO4的物质的量为: mol(用含有m、n的代数式表示)。
今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、Al3+、Fe3+、Mg2+、Ba2+、NH4+、Cl-、CO32—、SO42—,现取两份100 mL溶液进行如下实验:
①第一份加过量NaOH溶液加热后,只收集到气体0.02 mol,无沉淀生成,同时得到溶液甲。
②在甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧,质量为1.02 g。
③第二份加足量BaCl2溶液后,得白色沉淀,沉淀经足量盐酸洗涤、干燥后,质量为11.65 g。
根据上述实验回答:
(1)一定不存在的离子是 。
(2)试确定溶液中一定存在的阴离子及其物质的量浓度(可不填满):
(3)试确定K+是否存在 (填“是”或“否”),判断的理由是 。
实验室用如下图所示装置验证苯与溴反应的产物以及反应类型。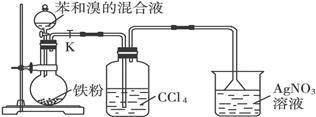
(1)由分液漏斗往烧瓶中滴加苯与溴的混合液时,反应很剧烈,可明显观察到烧瓶中充满了______________色气体。反应方程式: ;
(2)洗气瓶中产生的现象是: ,四氯化碳的作用是: ,如果省略洗气瓶, (填“能”或“不能”得到正确结论;
(3)则烧杯中产生的现象: ,说明苯与溴的反应是 反应;
(4)用离子方程式表示除去溴苯中溶解的溴: 。