某校化学探究小组探究有机化合物A的结构简式,其基本过程如下:
(1)取4.2g该有机化合物燃烧,将燃烧产物依次通入浓硫酸、足量澄清石灰水溶液,实验后,浓硫酸增重1.8g,生成碳酸钙的质量为20g,由此可确定A的最简式为_________。
(2)由质谱分析测定出A的相对分子质量为84,由此可确定A的分子式为_________。
(3)取8.4gA和足量银氨溶液反应,最终生成43.2g银,由此可确定A的结构简式为_____。
直接生成碳-碳键的反应是实现高效、绿色有机合成的重要途径。交叉脱氢偶联反应是近年备受关注的一类直接生成碳-碳键的新反应。例如:
化合物Ⅰ可由以下合成路线获得: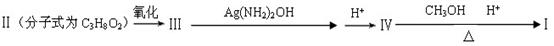
(1)化合物Ⅰ的分子式为____________,其完全水解的化学方程式为_____________(注明条件)。
(2)化合物Ⅱ与足量浓氢溴酸反应的化学方程式为_____________(注明条件)。
(3)化合物Ⅲ没有酸性,其结构简式为____________;Ⅲ的一种同分异构体Ⅴ能与饱和NaHCO3溶液反应放出CO2,化合物Ⅴ的结构简式为___________________。
(4)反应①中1个脱氢剂Ⅵ(结构简式如下)分子获得2个氢原子后,转变成1个芳香族化合物分子,该芳香族化合物分子的结构简式为_________________。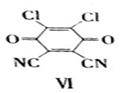
(5)1分子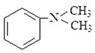 与1分子
与1分子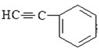 在一定条件下可发生类似反应①的反应,其产物分子的结构简式为____________;1mol该产物最多可与______molH2发生加成反应。
在一定条件下可发生类似反应①的反应,其产物分子的结构简式为____________;1mol该产物最多可与______molH2发生加成反应。
已知某燃料含碳、氢、氧三种元素,为了测定该燃料的组成:将该燃料放入足量氧气中燃烧,并使产生的CO2和H2O蒸气及剩余的O2全部通过如图所示的装置,得到如下表所列的实验数据(假设生成的气体全部被吸收)。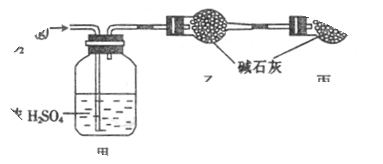
| 实验前 |
实验后 |
|
| 甲的质量 / g |
101.1 |
103.8 |
| 乙的质量 / g |
82.0 |
86.4 |
根据实验数据填空:
(1)该燃料分子中碳、氢原子的数目比为 。
(2)已知该燃料分子的式量为46,且每个分子中含有1个氧原子,则其分子式为
Ⅰ.中学课本中介绍了如下实验:把一端弯成螺旋状的铜丝放在酒精灯外焰加热,待铜丝表面变黑后立即把它插入盛有约2 mL乙醇的试管里,反复操作几次。
请你评价若用上述方法制取乙醛存在哪些不足(写出一点即可)。
Ⅱ.某课外活动小组利用下图装置进行乙醇的催化氧化实验并制取乙醛,图中铁架台等装置已略去,粗黑线表示乳胶管。请填写下列空白: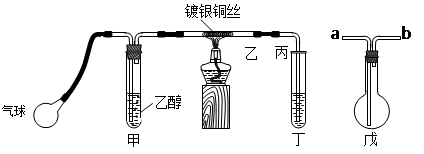
(1)甲装置常常浸在70~80℃的水浴中,目的是。
(2)若试管丁中用水吸收产物,则要在导管乙、丙之间接上戊装置,其连接方法是(填戊装置中导管代号):乙接、_______接丙;若产物不用水吸收而是直接冷却,应将试管丁浸在 _____中。
X、Y、Z、W为电子数相同的分子或离子。X有5个原子核。通常状况下,W为无色液体。它们之间转化关系如图所示,请回答:
(1)工业上每制取1molZ要放出46.2 kJ的热量,写出该反应的热化学方程式:。
(2)实验室制取Z的方法不止一种,写出其中一种方法的化学方程式:。
(3)某化学小组同学模拟工业生产制取HNO3,设计下图所示装置,其中a为一个可持续鼓入空气的橡皮球。
①A中发生反应的化学方程式是。
②B中浓H2SO4的作用是。
(4)写出D装置中反应的化学方程式。
(5)向含有ag HNO3的稀溶液中,加入bg铁粉充分反应,铁粉全部溶解。已知 ,则被还原的HNO3的质量为g。
,则被还原的HNO3的质量为g。
(8分)现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
甲同学:向1 mol·L-1的FeCl3溶液中加少量NaOH溶液。
乙同学:直接加热饱和FeCl3溶液。
丙同学:向25 mL沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热。
试回答下列问题:
⑴其中操作正确的同学是________。
⑵证明有Fe(OH)3胶体生成利用的胶体性质是________。
⑶在胶体中加入电解质溶液或带有相反电荷的胶体微粒能使胶体微粒沉淀出来。丁同学利用所制得的Fe(OH)3胶体进行实验:
①将其装入U形管内,用石墨作电极,通电一段时间后发现与电源负极相连的电极区附近的颜色逐渐变深,这表明Fe(OH)3胶体微粒带__________(填“正”或“负”)电荷。
②若向其中加入饱和Na2SO4溶液,产生的现象是。
③若向其中加入浓盐酸溶液,产生的现象是。
(4)Fe(OH)3胶体制备的化学方程式为。