综合利用海水可以制备食盐、纯碱、金属镁等物质,其流程如下图所示: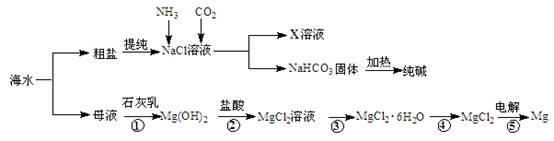
(1)反应①~⑤中,属于氧化还原反应的是 (填编号)。
(2)写出反应②的离子方程式 。
(3)X溶液中的主要阳离子是Na+和 。
(4)粗盐中含有Na2SO4、MgCl2、CaCl2等可溶性杂质,为制得纯净的NaCl晶体,操作如下:
①溶解;②依次加入过量的BaCl2溶液、NaOH溶液、Na2CO3溶液;③ ;④加适量盐酸;⑤ 。(请补全缺少的实验步骤)
(5)检验纯碱样品中是否含NaCl应选用的试剂是 。
根据下列的有机物合成路线回答问题: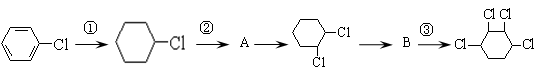
(1)写出A、B的结构简式:
A、B。
(2)写出各步反应类型:
①、②、③。
(3)写出②、③的反应方程式:
②,③。
(12分)今有化合物: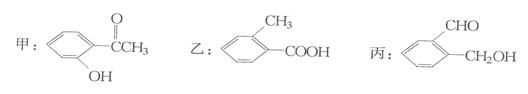
(1) 请判别上述哪些化合物互为同分异构体:。
(2) 请分别写出鉴别甲、乙的方法。(指明所选试剂及主要现象即可)
鉴别甲的方法:;
鉴别乙的方法:;
(3)鉴别丙的方法可以让其与银氨溶液反应,请写出该反应的化学方程式:。
(4)请按酸性由强至弱排列甲、乙、丙的顺序:。
等物质的量的甲烷、乙烯、乙炔、苯等四种有机物分别完全燃烧,需要O2最多的是 ;等质量的上述四种物质分别完全燃烧,需要O2最多的是_________。
某烃化学式为C8H10能使酸性KMnO4溶液褪色,溴水不能褪色,该烃具有_______种同分异构体,其中苯环上的一氯代物只有一种,该烃的名称为__________。
(14分) 分别由C、H、O三种元素组成的有机物A、B、C互为同分异构体,它们分子中C、H、O元素的质量比为15︰2︰8,其中化合物A的质谱图如下。
A是直链结构,其核磁共振氢谱有三组峰,且峰面积之比为1︰1︰2,它能够发生银镜反应。B为五元环酯。C的红外光谱表明其分子中存在甲基。其它物质的转化关系如下:
⑴A的分子式是:。A分子中的官能团名称是:。
⑵B和G的结构简式分别是:、。
⑶写出下列反应方程式(有机物用结构简式表示)
D→C;
H→G。
⑷写出由单体F分别发生加聚反应生成的产物和发生缩聚反应生成的产物的结构简式:、。