资源化利用二氧化碳不仅可减少温室气体的排放,还可重新获得燃料或重要工业产品。
(1)有科学家提出可利用FeO吸收和利用CO2,相关热化学方程式如下:6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) △H="-76.0" kJ·mol一1
①上述反应中每生成1 mol Fe3O4,转移电子的物质的量为_______mol。
②已知:C(s)+2H2O(g)=CO2(g)+2H2(g) △H="+113.4" kJ·mol一1,则反应:3FeO(s)+ H2O(g)= Fe3O4(s)+ H2(g)的△H=__________。
(2)在一定条件下,二氧化碳转化为甲烷的反应如下:CO2(g)+4 H2 (g)  C H4 (g)+2 H2O(g),向一容积为2 L的恒容密闭容器中充人一定量的CO2和H2,在300℃时发生上述反应,达到平衡时各物质的浓度分别为CO2 0.2 mol·L一1,H2 0.8 mol·L一1,CH40.8 mol·L一1,H2O1.6 mol·L一1。则CO2的平衡转化率为________。300 ℃时上述反应的平衡常数K=____________________。200℃时该反应的平衡常数K=64.8,则该反应的△H_____(填“>’’或“<”)O。
C H4 (g)+2 H2O(g),向一容积为2 L的恒容密闭容器中充人一定量的CO2和H2,在300℃时发生上述反应,达到平衡时各物质的浓度分别为CO2 0.2 mol·L一1,H2 0.8 mol·L一1,CH40.8 mol·L一1,H2O1.6 mol·L一1。则CO2的平衡转化率为________。300 ℃时上述反应的平衡常数K=____________________。200℃时该反应的平衡常数K=64.8,则该反应的△H_____(填“>’’或“<”)O。
(3)华盛顿大学的研究人员研究出一种方法,可实现水泥生产时CO2零排放,其基本原理如
图所示:
①上述生产过程的能量转化方式是____________________。
②上述电解反应在温度小于900℃时进行,碳酸钙先分解为CaO和CO2,电解质为熔融碳酸钠,则阳极的电极反应式为___________________。
下列物质能导电的是,属于电解质的是,属于非电解质的是。
①铜 ②碳酸钙 ③氯化钠晶体 ④稀硫酸
⑤干冰 ⑥蔗糖⑦ 盐酸 ⑧熔融态硫酸钡 ⑨HNO3
按要求回答问题:
(1)写出对应的化学方程式:
Cu2++Fe=Cu+Fe2+_________________________
CO32-+2H+ =CO2↑+H2O__________________________
(2)写出对应的离子方程式:
碳酸氢钙溶液与氢氧化钠溶液反应_________________
铁与氯化铁溶液反应
(3)写出下列物质的电离方程式:
硫酸铝电离的电离方程式:
KHCO3电离的电离方程式:
(4)用双线桥法标出电子转移的方向和数目:
2FeCl3 + 2KI = 2FeCl2 + 2KCl + I2
5NH4NO3 = 4N2↑+ 9H2O + 2HNO3
已知A、B、C、D分别是由短周期元素原子组成的四种微粒,它们之间有如图所示的转变关系,且A是种含有18电子的微粒,C是一种含有10电子的微粒。请完成下列各题: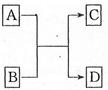
(1)若A、D分别是两种气态单质分子,写出A与B反应的化学方程
式
(2)若B、D属同主族的单质分子,写出C的化学式
(3)若B是一种含四核l8电子的分子,如果D是一种气态单质分子,B的结构简式为;
(4)若A、B均是含2个原子核的微粒,其中B中含有10个电子,D中含有18个电子,则A、B之间发生的离子反应方程式为
(5)若D是一种含有22电子的分子,则符合如图关系的A的物质有(写出物质的化学式,如果是有机物则写相应的结构简式)。
(共15分)X、Y、Z、L、M五种元素的原子序数依次增大,X的阴离子与Y的内层电子数相等,Y原子的最外层电子数是次外层电子数的两倍,Z、L是空气中含量最多的二种元素,M是地壳中含量最高的金属元素。回答下列问题:
(1)L的元素名称为;五种元素的原子半径从小到大的顺序是(用元素符号表示)。
(2)Z、X两元素按原子数目比1:3和2:4构成分子A和B,用电子式表示A的形成过程,B的结构式。
(3)硒(Se)是人体必须的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为,其最高价氧化物对应的水化物化学式为。该族2~5周期元素单质分别与H2反应生成1 mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是(填字母代号)。
a.+99.7 kJ·mol-1 b.+29.7 kJ·mol-1 c.-20.6 kJ·mol-1 d.-241.8 kJ·mol-1
(4)一定条件下,M与TiO2、C(石墨)反应只生成乙和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分。已知。该反应生成lmol乙时放出536kJ热量,其热化学方程式为
(7分)化合物A是尿路结石的主要成分,属于结晶水合物,可用X·nH2O表示。在一定条件下有如下图所示的转化关系: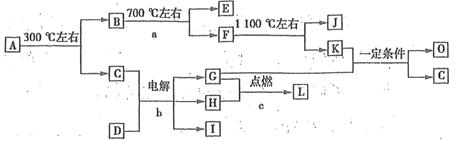
已知:①上图中的各字母代表的物质均由常见元素(原子序数≤20)组成,其中X由三种元素组成;A、D晶体中阴、阳离子个数比都是l:1;D中的阳离子与C分子有相同的电子数,A中的阳离子与D中的阴离子的电子层结构相同。
②G、H是常见的气体单质,E、K、L是常见的气体化合物;E被人体吸入,会与血红蛋白结合而使人中毒,K的大量排放是造成地球温室效应的主要原因。
③反应b、c是重要的化工反应,I是一种重要的化工原料。
④转化关系图中的部分变化经定量测定,得到如右图所示的固体产物的质量分数[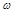 (%)]随温度[T(℃)]的变化曲线。
(%)]随温度[T(℃)]的变化曲线。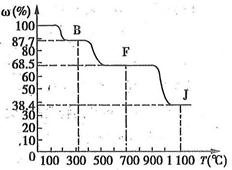
回答下列问题:
(1)写出A的化学式:,D阴离子的示意图。
(2)反应a的化学方程式为。
(3)写出电解反应b的化学方程式,并标出电子转移的方向和数目:。
(4)K与G在一定条件下可生成多种物质,既可获得经济效益,也可减少对环境的污染。若O是一种易挥发的液态燃料,有毒,误饮5~10mL会导致双目失明。则O的分子式为。