水的电离过程为:H2O H++OH-,在不同温度下其平衡常数为Kw(25 ℃)=1.0×10-14,Kw(35 ℃)=2.1×10-14。则下列叙述正确的是
H++OH-,在不同温度下其平衡常数为Kw(25 ℃)=1.0×10-14,Kw(35 ℃)=2.1×10-14。则下列叙述正确的是
| A.c(H+)随着温度升高而降低 | B.在35℃时,c(H+)>c(OH-) |
| C.蒸馏水中通HCl, Kw增大 | D.水的电离为吸热过程 |
下列物质不耐酸雨腐蚀的是
| A |
B |
C |
D |
 |
 |
 |
 |
| SiO2 -光导纤维 |
聚氯乙烯 -输液管 |
酚醛树脂 -飞船仓外层 |
锰钢 -钢轨 |
某溶液中可能含有Na+、K+、AlO2-、CO32-、SO32-、Cl-中的若干种离子。某同学设计并完成了如下实验: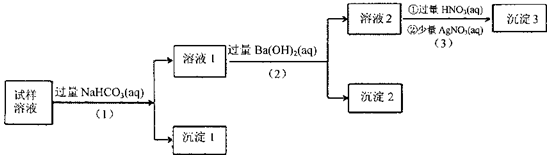
已知:AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-
根据以上的实验操作与现象,该同学得出的结论不正确的是
| A.沉淀2放置在空气中,若质量增加,试样中肯定存在SO32- |
| B.试样溶液中加人稍过量的NH4C1溶液能得到与沉淀1成分相同的物质 |
| C.上述流程步骤(1)(2)(3)的顺序改为(3)(2)(1),可能会获得相同的实验现象 |
| D.试样溶液中肯定存在AlO2-、Cl-,其中Na+、K+至少存在1种 |
在25°C时,向10mL0.0lmol·L-1NaCN溶液中逐滴加人0.0lmol·L-1的盐酸,滴定曲线如图1所示,CN—、HCN浓度所占分数(α)随pH变化的关系如图2所示,下列表述正确的是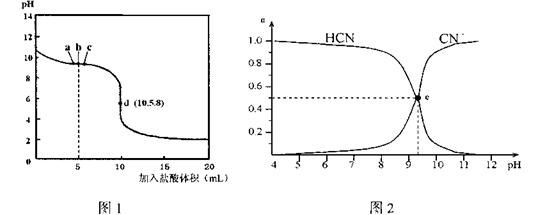
| A.b点时,溶液中微粒浓度大小的关系:c(CN-)>c(Cl-)>c(HCN)>c<(OH-)>c(H+) |
| B.d点溶液存在的关系:c(Na+)+c(H+)=c(HCN)+c(OH-)+2c(CN-) |
| C.图2中的e点对应图1中的c点 |
| D.在滴定过程中选用酚酞试剂比选用甲基橙试剂作指示剂误差更小 |
化学镀铜废液中含有一定量的CuSO4,任意排放会污染环境,利用电化学原理可对废液进行回收处理,装置如图,其中质子交换膜只允许H+通过。已知:①Cu2++ HCHO + 3OH-=Cu + HCOO-+ 2H2O;②还原性:HCHO > M(—种金属)> Cu。
下列说法正确的是
| A.反应之前,应将含OH-的HCHO溶液加人到装置的左侧 |
| B.右侧发生的电极反应式:HCHO-2e-+H2O=HCOO-+3H+ |
| C.若将质子交换膜换成阴离子交换膜,放电过程中,大量的OH-将向左侧迁移 |
| D.放电一段时间后打开开关,移去质子交换膜,装置中可能会有红色固体、蓝色絮状物出现 |
下列说法正确的是
A.按系统命名法,化合物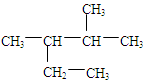 的名称为2-甲基-3-乙基丁烷 的名称为2-甲基-3-乙基丁烷 |
| B.甲醇、乙醇、甘油互为同系物 |
C.等物质的量的乙炔、乙醛、 完全燃烧时耗氧量不相等 完全燃烧时耗氧量不相等 |
| D.以乙烯为原料制备乙酸乙酯的合成路线可以为: |
