常温下,pH=11的氨水和pH=1的盐酸等体积混合(混合溶液体积为两溶液体积之和),恰好完全反应,则下列说法错误的是
| A.氨水的浓度大于盐酸的浓度 |
| B.原氨水中有1%的含氮微粒为NH4+ |
| C.氨水中水电离出的c(H+)是盐酸中水电离出的c(H+)的100倍 |
| D.混合溶液中c(NH4+)+c(NH3·H2O)+c(NH3)=5×10-4mol/L |
下列化学式只表示一种分子的是
| A.C2H6O | B.(C6H10O5)n | C.—CH2CH3 | D.C2H4 |
2.某化学反应其ΔH =-125 kJ/mol,∆S =" 81" J/(mol·K),则此反应在下列哪种情况下可自发进行
| A.在任何温度下都能自发进行 | B.在任何温度下都不能自发进行 |
| C.仅在高温下自发进行 | D.仅在低温下自发进行 |
下列有关煤的说法中不正确的是
| A.煤是工业上获得芳香烃的重要来源 |
| B.开发新能源,减少燃煤,是控制酸雨,保护环境的有效途径之一 |
| C.煤、石油、水煤气均是可再生能源 |
| D.煤的干馏和石油的裂解过程均属于化学变化过程 |
常温下,用0.1000 mol/L HCl溶液滴定20.00 mL 0.1000 mol/L NH3•H2O溶液,滴定曲线如下图。下列说法正确的是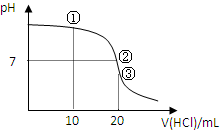
| A.①溶液:c(C1—)>c(NH4+)>c(OH—)>c(H+) |
| B.②溶液:c(NH4+)=c(C1—)>c(OH—)=c(H+) |
| C.③溶液:c(H+)>c(NH3·H2O) + c(OH—) |
| D.滴定过程中可能出现:c(NH3•H2O)>c(NH4+)>c(OH—)>c(Cl—)>c(H+) |
关于下列各实验装置的叙述中,不正确的是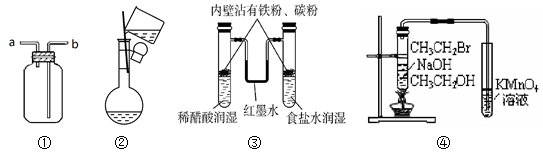
| A.装置①:a口进气可收集CO2,b口进气可收集NH3 |
| B.装置②:配制一定物质的量浓度溶液时,转移溶液 |
| C.装置③:模拟铁锈蚀 |
| D.装置④:证明CH3CH2OH发生消去反应生成了乙烯 |