Ⅰ.合理饮食和正确用药,是人体健康的重要保证。
现有下列五种物质A食盐;B小苏打;C苹果汁;D葡萄糖;E青霉素,请按下列要求填空(填序号)。
富含维生素C的是 ,可直接进入血液,补充能量的是 ,应用最广泛的抗生素之一的是 ,既可作为疏松剂,又可治疗胃酸过多的是 ,食用过多会引起血压升高、肾脏受损的 。
Ⅱ.钢铁的生产与使用是人类文明和生活进步的一个重要标志。
(1)写出工业上用赤铁矿炼铁的主要化学反应方程式: 。
(2)炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会因腐蚀出现红褐色锈斑。试回答:
①铁锅的腐蚀主要是由 (填化学或电化学)腐蚀造成的。形成的铁锈的主要成分是 。
②为防止轮船的船体在海水中腐蚀,一般在船身连接 (填“锌块”或“铜块”)。
Ⅲ.材料是人类赖以生存和发展的重要物质基础,合理使用材料可以改善我们的生活。
(1)体育场馆建设需大量建筑材料。下列材料不属于硅酸盐材料的是 (填字母)。
A.石灰石 B.水泥 C.玻璃
(2)在下列材料中,属于无机非金属材料的是 (填字母)。属于塑料制品的是 。
A.涤纶 B.聚氯乙烯塑料 C.氮化硅陶瓷 D.玻璃钢
(3)下列有关合金性质的说法正确的是 (填字母)。
A.合金的熔点一般比它的成分金属高
B.合金的硬度一般比它的成分金属低
C.组成合金的元素种类相同,合金的性能就一定相同
D.合金与各成分金属相比,具有许多优良的物理、化学或机械性能
(4)合成塑料、合成橡胶和 是常说的三大合成材料。
(共14分)下表是元素周期表中的一部分,根据A—I在周期表中的位置,用元素符号或化学式回答下列问题:
 |
ⅠA |
0 |
||||||
| 1 |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
||
| 2 |
D |
E |
G |
I |
||||
| 3 |
A |
B |
C |
F |
H |
(1)表中元素,化学性质最不活泼的是,氧化性最强的单质是,还原性最强的单质是;
(2)最高价氧化物的水化物碱性最强的是,酸性最强的是,呈两性的是;
(3)要证明A、B、C的金属活泼性,可以用什么实验来证明,试举一例
实验操作;
实验现象:;
有关化学方程式:
(4)G与H的气态氢化物稳定性>,说明相应单质的非金属性>。
已知A~O分别代表一种物质,它们之间的转化关系如下图所示(反应条件略去)。A、B、H分别是由短周期元素组成的单质。B与冷水缓慢反应,与沸水迅速反应放出氢气。D是一种离子化合物,其阴阳离子的个数之比为2:3,且能与足量的水反应得到两种碱。C为淡黄色固体化合物,物质O能与G的水溶液反应生成蓝色沉淀。
(1)组成H单质的元素位于周期表第周期,第族;
(2)化合物D的化学式为;
(3)物质F的水溶液与G的水溶液在常温下反应的离子方程式为:;
(4)物质C与等物质的量的KHSO3溶液反应的离子方程式为:;
(5)物质N的浓溶液与Cu反应的化学方程式:。
双安妥明是一种降血脂药物,主要用于降低血液中胆固醇浓度,安全,副作用小,其结构简式为:
已知 : I
II.
双安妥明的合成路线如下
已知:C的分子式为C4H8,且支链有一个甲基;Ⅰ能发生银镜反应且1mol I能与2mol氢气发生加成反应;K的结构具有对称性。试回答下列问题:
①写出结构简式:A, J,
C的名称为。
②反应(2)的条件是,反应(3)的类型是。
③写出反应(4)的化学方程式:
④与F互为同分异构体,且属于酯类的有机物有种,并写出其中能发生银镜反应的有机物的结构简式:。
一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)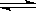 CH3OH(g) ΔH< 0
CH3OH(g) ΔH< 0
根据题意完成下列各题:
(1)反应达到平衡时,平衡常数表达式K=。
(2)其它条件不变,仅把温度改为500℃,请在下图上画出此温度下甲醇的物质的量随反应时间变化的示意图。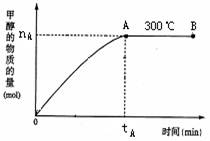
(3)升高温度,K值(填“增大”、“减小”或“不变”),增大压强,
K值(填“增大”、“减小”或“不变”)。
(4)在300℃,从反应开始到平衡,氢气的平均反应速率v(H2)=
(5)在其他条件不变的情况下,对处于B点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是()
a.氢气的浓度减少 b.正反应速率加快,逆反应速率减小
c.甲醇的物质的量增加 d.重新平衡时n(H2)/n(CH3OH)减小
已知A、B、C、D、E五种元素为前20号元素,其原子序数依次增大,A元素所处的周期数、主族序数、原子序数均相等;B元素与A元素形成的一种式量为32的化合物常做火箭的推进剂,其另一种化合物的水溶液能使红色石蕊试纸变蓝;E元素的原子半径在前20号元素中最大(不含稀有气体);D元素与A元素能形成分子式为AD典型的共价化合物;C元素的单质和氧化物均能既溶于AD的水溶液,也能溶于E元素最高价氧化物对应的水化物。试回答:
(1)元素符号:A____,B_____,E。
(2)比较C、D、E三种元素简单离子的半径大小关系:(离子符号表示)
(3)鉴别E元素存在的方法是:;
(4)写出C元素的离子与过量E元素的最高价氧化物对应的水化物的离子方程式:
;
(5)写出A、B两元素形成的式量为32的化合物的电子式;若0.5mol该气态化合物与N2O4(g)充分反应生成无毒的气态产物所放出的热量为269.175KJ,请写出该反应的热化学方式:。