如图所示,a、b、c均为石墨电极,d为碳钢电极,通电电解一段时间。假设在电解过程中产生的气体全部逸出,下列说法正确的是
| A.甲、乙两烧杯中溶液的pH均保持不变 |
| B.甲烧杯中a电极反应式为:4OH――4e-=O2↑+2H2O |
| C.当电解一段时间后,将甲、乙两溶液混合,一定会产生蓝色沉淀 |
| D.当b极增重3.2 g时,d极产生的气体为0.56 L(标准状况) |
2011年10月16日,嘉兴的空气质量日报通报嘉兴市区的SO2、NO2、可吸入颗粒物污染指数分别为60,70,90,则嘉兴的空气质量等级是:
| A.优 | B.良 | C.轻微污染 | D.轻度污染 |
下列关于晶体说法的正确组合是 
①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低
④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
⑤CaTiO3晶体中(晶胞结构如上图所示)每个Ti4+和12个O2-紧邻
⑥SiO2晶体中每个硅原子与两个氧原子以共价键相结合
⑦晶体中分子间作用力越大,分子越稳定
⑧氯化钠熔化时离子键被破坏
A.①②③⑥ B.①②④
C.③⑤⑦D.③⑤⑧
非整比化合物Fe0..95O具有NaCl型晶体结构。由于n (Fe)∶n (O)<1,所以晶体存在缺陷。Fe0..95O可表示为
A.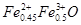 |
B.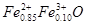 |
C.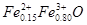 |
D. |
下列气体的制备可采用右图装置的是 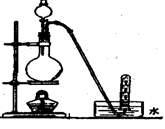
| A.铜与浓硝酸反应制NO2 |
| B.铜与稀硝酸反应制NO |
| C.乙醇与浓硫酸反应制乙烯 |
| D.石灰石和盐酸 |
在密闭容器中,1mol HI分解[2HI(g)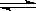 H2(g)+I2(g)]时,I2的体积分数为X%;相同条件下,2 mol HI分解达平衡时,I2的体积分数为Y%,则X与Y的关系为
H2(g)+I2(g)]时,I2的体积分数为X%;相同条件下,2 mol HI分解达平衡时,I2的体积分数为Y%,则X与Y的关系为
| A.X<Y | B.X=Y | C.X>Y | D.X=Y/2 |