氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一。
(1)上图是1 mol NO2气体和1 mol CO气体反应生成CO2气体和NO气体过程中能量变化示意图,请写出NO2和CO反应的热化学方程式: ;
已知:N2 (g)+2NO2 (g)  4NO(g) △H=+292.3kJ·mol—1,
4NO(g) △H=+292.3kJ·mol—1,
则反应: 2NO(g)+2CO(g) N2(g)+2CO2(g) 的△H= ;
N2(g)+2CO2(g) 的△H= ;
(2)一定温度下,在体积为2L的恒容密闭容器中充入20 mol NO2和5 mol O2发生反应: 4NO2(g)+O2(g) 2N2O5(g);已知体系中n(NO2)随时间变化如下表:
2N2O5(g);已知体系中n(NO2)随时间变化如下表:
| t(s) |
0 |
500 |
1000 |
1500 |
| n(NO2)(mol) |
20 |
13.96 |
10.08 |
10.08 |
①写出该反应的平衡常数表达式:K= ,已知:K3000C>K3500C,则该反应是 反应(填“放热”或“吸热”);
②反应达到平衡后,NO2的转化率为 ,若要增大NO2的转化率,可采取的措施有
A.降低温度
B.充入氦气,使体系压强增大
C.再充入NO2
D.再充入4 mol NO2和1 mol O2
③图中表示N2O5的浓度的变化曲线是 ,用O2表示从0~500s内该反应的平均速率v= 。
已知A、B、C、D、E是短周期中的5种非金属元素,它们的原子序数依次增大。A元素原子形成的阳离子核外电子数为零,B原子的最外层电子数是内层电子数的2倍。C、D在元素周期表中处于左右相邻的位置,它们的单质是空气的主要成分, E元素与D元素同主族。
(1) 请写出元素符号:A_______, E______。
(2) C的气态氢化物的水溶液呈_______ 性(填“酸”、“碱”或“中”),写出C的气态氢化物的电子式_____________,以及与HCl形成的盐的化学式______________ 。
⑶A、B两元素形成的相对分子质量最小的有机物的分子式,空间构型是。
A是面粉中的主要成分,C与E反应可生成F,D能与新制的Cu(OH)2悬浊液反应产生砖红色沉淀。下图是A、B、C、D、E、F等几种常见有机物之间的转化关系图: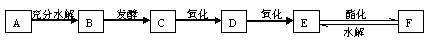
根据以上信息完成下列各题:
(1)A的化学式为____________,B的名称为_____________。
(2)C的结构简式为__________,D的结构简式为__________,F的结构简式为__________。
(3)C和E反应生成F的化学方程式为_________________________________。
(4)E与小苏打溶液反应的化学方程式为_______________________________________。
Ⅰ.可逆反应:A(g)+3B(g) 2C(g)+3D(g),取1 mol A和2 mol B置于2L容器内。1分钟后,测得容器内A的浓度为0.2 mol/L。
2C(g)+3D(g),取1 mol A和2 mol B置于2L容器内。1分钟后,测得容器内A的浓度为0.2 mol/L。
(1)这时B的浓度为________mol/L,C的浓度为________mol/L。
(2)这段时间内反应的平均速率若以D的浓度变化来表示,应为________mol/(L·min)。
(3)如果保持容器内温度不变,反应前和反应后容器内压强之比为_____(最简整数比)。
Ⅱ.电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液。请回答以下问题:
(4)在X极附近观察到的实验现象是:放出气体且______________。检验Y电极反应产物的方法是:把__________________放在Y电极附近,试纸变蓝色。
(5)当通过电解池通过1 mol电子时,两极共收集到________L气体(标准状况),电解池内的液体稀释到500 mL时,NaOH溶液浓度为________mol/L。
Ⅰ.在1~18号元素中,回答下列问题,答案要求写出化学式。
(1)最高价氧化物的水化物碱性最强的物质是______________,最高价氧化物的水化物酸性最强的物质是______________,气态氢化物最稳定的是______________。
Ⅱ.已知X、Y、Z是三种短周期元素,且原子序数按X、Y、Z的顺序依次增大,且原子序数之和为33,最外层电子数之和为11,在周期表中,X、Z上下相邻,Y、Z左右相邻。
(2)X、Y、Z的元素符号分别为___________、___________、___________。
(3)X和Z分别能与氧形成XO2和ZO2,XO2在固态时属于___________晶体,ZO2在固态时属于___________晶体。
酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业,乙酸乙酯的实验室和工业制法常采用如下反应: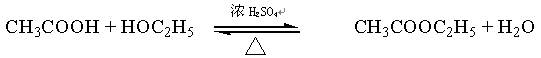
请根据要求回答下列问题:
(1)欲提高乙酸的转化率,可采取的措施有,。(任写两点只要合理即可)
(2)浓硫酸的作用是:①、②。
(3)饱和NaCO3溶液的作用:
(4)目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可用作此反应的催化剂,且能重复使用。实验数据如下表所示(乙酸和乙醇以等物质的量混合)
| 同一反应时间 |
同一反应温度 |
||||
| 反应温度/℃ |
转化率/% |
选择性/% |
反应时间/h |
转化率/% |
选择性/% |
| 40 |
77.8 |
100 |
2 |
80.2 |
100 |
| 60 |
92.3 |
100 |
3 |
87.8 |
100 |
| 80 |
92.6 |
100 |
4 |
92.3 |
100 |
| 120 |
94.5 |
98.7 |
6 |
93.0 |
100 |
| 选择性100%表示反应无副反应发生 |
根据表中数据,下列(填字母)为该反应的最佳条件。
| A.120 ℃,4 h | B.80 ℃,2 h | C.60 ℃,4 h | D.40 ℃,3 h |