铁质水龙头长期使用容易生锈,小明从自家水龙头上取下一些铁锈样品,用图甲所示的装置进行实验。 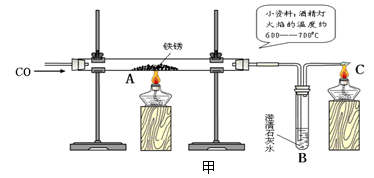
(1)B处澄清石灰水变浑浊,反应方程式为 ,C处酒精灯的作用是
(2)实验结束,小明将所得的黑色固体物质放入足量的稀硫酸中,发现没有气泡,这说明生成物中 (有或没有)铁。
为解释这个现象,小明查阅下列资料:
Ⅰ.已知铁的氧化物有FeO、Fe3O4、Fe2O3,,在一定条件下,均能逐步失去其中的氧,最终被还原为铁。
Ⅱ.某炼铁厂对氧化铁和一氧化碳进行热反应分析,获得相关数据并绘制成下图。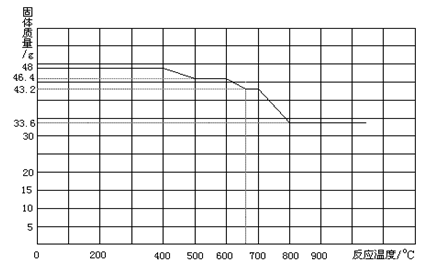
通过分析资料确定:
①700℃时氧化铁和一氧化碳进行反应的产物是 (填FeO或Fe3O4或Fe).
②小明实验失败的主要原因是 。
现有失去标签的5种无色溶液,分别是Na2CO3、NaCl、Ca(OH)2、NaOH和稀盐酸,任取其中的4种贴上A、B、C、D标签,进行如下实验.
(1)依据如图装置进行实验,其中夹持固定装置已略去.从长颈漏斗加入稀盐酸,可以观察到C溶液中有气泡产生,A溶液中有白色沉淀生成,B、D溶液均无明显变化.则C溶液与稀盐酸反应的化学方程式为;A溶液中发生反应的化学方程式为.
(2)取少量B溶液倒入蒸发皿,加热,闻到有刺激性气味,停止加热.再取少量D溶液倒入另一蒸发皿,加热,有白色固体析出,停止加热.则B是.
(3)同学们认为实验(1)反应后的D溶液中溶质的成分有多种可能,请你设计实验方案证明。 
小红为大家做了一个“燃纸成铁”的趣味实验.将一张滤纸(组成元素为C、H、O)用FeCl3浓溶液润湿,在酒精灯上烘干后点燃,滤纸变黑、红热,最终生成黑褐色物质.小红告诉大家:黑褐色物质中含有铁单质.
【提出问题】黑褐色物质中真的含有铁单质吗?
【探究过程】
(1)小红先从反应物分析,因为所以反应后可能生成铁单质.
(2)为获得实验证据,小红做了实验1.
实验1:将黑褐色物质放入稀盐酸中,发现有连续微小气泡产生.若黑褐色物质中含有铁单质,则反应的化学方程式为.
(3)小明提出疑问:由反应物的组成分析,能与稀盐酸反应产生气泡的物质不一定是铁单质,还可能是.
小红通过查阅资料得知,在高温条件下不可能生成此类物质.
(4)小明仍有疑问:实验1中产生的气泡也可能是滤纸碳化后吸附的空气.为此,小红又做了实验2:观察到有微小气泡产生但很快停止.证明实验1中的连续气泡确实是由铁单质与稀盐酸反应产生的.
(5)为进一步证明黑褐色物质中有铁单质,小红又做了实验3.
实验3:将黑褐色物质放入溶液中,观察到.
【得出结论】通过以上实验探究,证明黑褐色物质中确实含有铁单质.
【实验反思】小红所做实验1和实验2用了对比实验,这种实验的要求是.
化学兴趣小组用如图所示装置研究两个问题:
(1)研究燃烧的条件【步骤2】打开K3,关闭K2,打开K1将A中溶液滴入Ⅰ中与B接触,关闭K1.Ⅲ中有气泡冒出,白磷燃烧.Ⅲ中发生反应的化学方程式为.此实验运用对比的方法研究了燃烧的一个条件,它是.
(2)研究二氧化碳与氢氧化钠的反应
A中盛有稀硫酸,B为碳酸钠固体,Ⅲ中盛有氢氧化钠溶液.
【实验1】打开K3,关闭K2,打开K1将A中溶液滴入Ⅰ中与B接触,关闭K1.一段时间后,Ⅲ中没有明显现象.
【实验2】证明二氧化碳与氢氧化钠发生了反应,Ⅱ中盛放的可能是,后续实验的操作及现象是.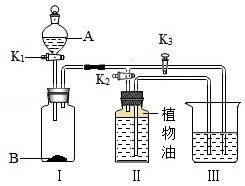
制作松花蛋的主要原料可能有生石灰、纯碱和食盐,化学兴趣小组为了确定该原料的成分,进行实验,记录如下:
| 实验操作 |
实验主要现象 |
|
| ① |
取少量原料样品于试管中,加入一定量的水充分溶解 |
溶液变浑浊,且有明显放热 |
| ② |
静置一段时间后,过滤,向滤液中加入过量的试剂A |
无明显变化 |
| ③ |
向白色固体中加入试剂B,将产生的气体通入试剂A |
白色固体消失,有气泡产生,试剂A变浑浊 |
根据以上实验现象,回答下列问题:
(1)操作①中,试管中发生反应的化学方程式为
(2)操作②中,滤液中一定不存在的溶质是,加入过量的试剂A后,溶液中一定存在的溶质是.
(3)进行操作③的目的是 ,试剂A变浑浊的原因是(用化学方程式表示)
(4)通过上述实验能够确定制作松花蛋的主要原料中,一定有的物是.
学校化学兴趣小组的同学知道二氧化锰能作过氧化氢(H2O2)分解的催化剂后,想再探究其他一些物质如氧化铝是否也可作过氧化氢分解的催化剂.请你一起参与他们的探究过程,并填写下列空白.
【提出问题】Al2O3能不能作过氧化氢分解的催化剂呢?
【作出猜想】Al2O3能作过氧化氢分解的催化剂。
【实验验证】
| 实验步骤 |
实验现象 |
实验结论 |
|
| 实验一 |
有少量气泡 木条不复燃 |
常温下过氧化氢溶液分解速率很慢. |
|
| 实验二 |
在装有过氧化氢溶液的试管中加入少量Al2O3,然后将带火星的木条伸入试管中 |
产生大量的气泡 木条复燃 |
【得出结论】Al2O3能加快过氧化氢的分解速率,故Al2O3能作过氧化氢分解的催化剂.
【反思提高】经过讨论,有的同学认为只有上述两个证据,不能证明Al2O3能作过氧化氢分解的催化剂,还要补充一个探究实验三:
实验三:
【实验目的】探究。
【实验步骤】①准确称量Al2O3(少量)的质量;
②完成实验二;
③待反应结束,将实验二试管里的物质进行过滤,洗涤,,称量;
④对比反应前后Al2O3的质量.
【交流讨论】如果Al2O3在反应前后质量不变,则说明Al2O3可以作过氧化氢分解的催化剂.
【提出新的问题】但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验四:
实验四的目的是探究。