下图装置可以完成多个简单实验,具有药品用量少、实验现象明显、尾气不外逸等优点。
小资料:Na2CO3 + H2SO4=Na2SO4 + H2O + CO2↑;
氧化钙(俗称生石灰)与水反应放热。
(1)若甲中吸有浓氨水,乙中吸有无色酚酞溶液,将甲、乙中的液体同时挤出,一段时间后,观察到无色酚酞溶液变红,说明分子具有的性质是________。
(2)若甲中吸有水,乙中吸有稀硫酸,烧杯①中盛有用石蕊溶液染成紫色的干燥纸花,烧杯②中盛有碳酸钠粉末。为了验证使石蕊变色的物质是碳酸而不是二氧化碳,应采取的实验操作是________。
(3)若先将甲中的液体挤出,观察到气球明显鼓起,一段时间后恢复原状;再将乙中的液体挤出,气球又明显鼓起。请将下表中的试剂补充完整。
| |
滴管甲 |
烧杯① |
滴管乙 |
烧杯② |
| 试剂 |
H2O |
|
|
MnO2 |
气球鼓起是因为装置内气压增大,两次气压增大的原因依次是________。
(9分)科学探究是奇妙的过程,请你一起参与下列有关过氧化氢溶液制备氧气的探究实验。
(1)问题1过氧化氢溶液分解速率与催化剂种类有关吗?
在常温下,在相同质量、相同浓度的过氧化氢溶液中,分别加入1g二氧化锰和x g氧化铜,测量各生成一瓶(相同体积)氧气所需的时间。实验数据记录如下:
| 实验编号 |
Ⅰ |
Ⅱ |
| 反应物 |
5%过氧化氢溶液 |
5%过氧化氢溶液 |
| 催化剂 |
1 g 二氧化锰 |
x g 氧化铜 |
| 时 间 |
46 s |
84 s |
上述实验中可用排水法收集氧气,理由是 。实验Ⅰ反应的文字表达式是 ,若实验时忘了加入二氧化锰固体,结果是 。实验Ⅱ中x的值应为 。本实验中,与发生装置连接用来测量O2体积的装置可以用下图中的 (填编号)。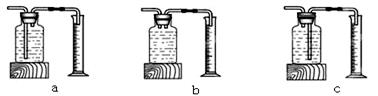
实验结论1: 。
(2)问题2过氧化氢溶液分解速率与反应物浓度有关吗?
实验数据记录如下:
| 双氧水的质量 |
双氧水的浓度 |
MnO2的质量 |
相同时间内产生O2体积 |
|
| Ⅰ |
50.0g |
1% |
0.1g |
9mL |
| Ⅱ |
50.0g |
2% |
0.1g |
16mL |
| Ⅲ |
50.0g |
4% |
0.1g |
31mL |
实验结论2:在相同条件下, 。
上述实验中除了量筒外还需用到的测量仪器有 (写出其中一种)。
(3)影响过氧化氢溶液分解速率可能还与温度有关,请设计实验方案进行验证: 。
下列是初中化学的两个实验,按要求回答问题:
(1)某课外活动小组设计测定空气中氧气含量的实验,实验装置如图所示: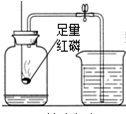
①红磷在集气瓶中发生反应的文字表达式为
该实验可观察到的现象为
该实验中红磷稍过量,目的是
②由实验现象可得出的结论是
(2)某课外活动小组设计如图装置研究分子的性质: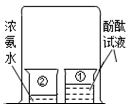
① 向盛有约20ml蒸馏水的小烧杯①中加入5~6滴酚酞溶液,搅拌均匀观察到溶液
② 从上述烧杯①中取少量溶液置于试管中,向其中慢慢滴加浓氨水,观察到溶液
③ 另取一个烧杯②(如图),加入约5ml浓氨水。用一个大烧杯罩住①②两个小烧杯。过了几分钟,观察到
综合②③实验说明分子
反思:为什么两个烧杯不同时变色呢?
查阅资料:不同的分子在相同的条件下运动速率不同。
由此可根据现象推断 分子运动速率快(填氨或酚酞)。
化学兴趣小组的三位同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究。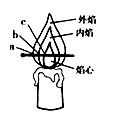
(1)贝贝取一支蜡烛,用小刀切下一小块,把它放入水中,蜡烛浮在水面上。结论:石蜡的密度比水_______;
(2)芳芳点燃蜡烛,观察到火焰分为外焰、内焰、焰心三层。把一根火柴梗放在火焰中(如上图所示)约1s后取出,可以看到火柴梗的________________(填“a”“b” 或“c”)处最先碳化。结论:蜡烛火焰的__________________温度最高;
(3)婷婷在探究蜡烛燃烧的过程中,发现罩在火焰上方的烧杯内壁被熏黑,你认为她的以下做法中不合适的是_________________。
| A.反复实验,并观察是否有相同现象 |
| B.查找资料,了解石蜡的主要成分,探究生成的黑色固体是什么 |
| C.认为与本次实验目的无关,不予理睬 |
| D.询问老师或同学,讨论生成黑色物质的原因 |
(4)三位同学在探究的过程中,将短玻璃导管插入焰心,发现另一端也可以点燃。
【提出问题】导管里一定有可燃性气体,气体成分可能会是什么呢?
【猜想】贝贝认为:可能是蜡烛不完全燃烧时产生的一氧化碳 (一氧化碳具有可燃性) 。
芳芳认为:可能是蜡烛受热后产生的石蜡蒸气。
婷婷认为:可能以上两种情况都有。
【实验方案】换一根较长的导管,并用冷的湿毛巾包住导管,然后在导管另一端做点火实验。
【现象与结论】
如果观察到 现象,则贝贝的猜想正确;
如果观察到 现象,则芳芳的猜想正确;
如果观察到 现象,则婷婷的猜想正确。
人教版新化学教材关于“分解过氧化氢制氧气的反应中二氧化锰的催化作用”,以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
【实验探究】
| 实验步骤 |
实验现象 |
| Ⅰ.分别量取5mL5%过氧化氢溶液放入A、B两支试管中,向A试管中加入ag氧化铁( Fe2O3)粉末,并分别在A、B两支试管中插入带火星木条,观察现象。 |
A试管中产生气泡,带火星木条复燃,B试管中无明显现象。 |
| Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次实验,观察现象。 |
试管中均产生气泡,带火星木条均复燃。 |
| Ⅲ.将实验Ⅱ中的剩余物小心过滤,并将所得虑渣进行洗涤、干燥、称量,所得固体质量仍为ag。 |
 |
| Ⅳ.分别量取5mL5%过氧化氢溶液放入C、D两支试管中,向C试管中加入ag氧化铁粉末.向D试管中加入ag二氧化锰粉末,观察现象。 |
 |
【实验结论】
(1)A中产生的气体是 。
(2)实验Ⅱ、Ⅲ证明:氧化铁(Fe2O3)的 和 在反应前后均没有发生变化,可以作过氧化氢分解的催化剂。
(3)写出氧化铁(Fe2O3)催化过氧化氢分解的化学符号表达式 。
【实验评价】
(1)设计实验Ⅳ的目的是 。
(2)若实验Ⅳ观察到D试管中产生气泡的速率更快,由此你可以得到的结论是 。
【实验拓展】
查阅资料得知:CuO、CuSO4、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是 。
A.MnO2只能作为过氧化氢溶液分解的催化剂
B.同一个化学反应可以有多种催化剂
C.催化剂只能加快化学反应的速率
D.用作催化剂的物质不可能是其它反应的反应物或生成物
以下是某研究小组探究影响化学反应快慢的一些因素的相关数据(常温通常指20℃;“浓度”指溶质的质量分数)
| 实验序号 |
过氧化氢溶液浓度/% |
过氧化氢溶液质量/g |
温度/0C |
二氧化锰用量/g |
氧气体积/ml |
反应所需时间/s |
| ① |
5 |
12 |
20 |
0.2 |
125 |
11 |
| ② |
30 |
12 |
20 |
0.2 |
125 |
2 |
| ③ |
30 |
12 |
40 |
/ |
125 |
148 |
| ④ |
30 |
12 |
90 |
/ |
125 |
82 |
(1)通过实验①和②对比可知,化学反应快慢与 有关;
(2)通过对比实验 和 可知,化学反应快慢与温度的关系是 .
(3)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是 .
(4)同种催化剂,还有哪些因素可能影响催化效果,请你再探究(探究一种因素即可)