某化学兴趣小组的同学利用下图所示实验装置进行某些气体的制备、性质等实验(图中夹持装置有省略)。请按要求填空:
Ⅰ.探究氯气与氨气的反应
(1)为制取干燥氨气,可将装置C与________(填装置编号)连接;装置C中的烧瓶内固体宜选用________。
a.碱石灰 b.氯化钙 c.五氧化二磷 d.生石灰
(2)装置A、E、E连接可制取纯净、干燥的氯气,则两个E装置内的药品依次是________________。
(3)装置F可用于探究氯气与氨气(已知氯气与氨气可发生反应:3Cl2+2NH3===N2+6HCl)的反应。实验时打开弹簧夹1、3,关闭2,先向烧瓶中通入________,然后关闭1、3,打开2,向烧瓶中缓慢通入一定量的另一种气体。实验一段时间后烧瓶内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案鉴定该固体中的阳离子______________________________________________________________________________。
Ⅱ.探究某些物质的性质
(4)利用装置A、E,可设计实验比较Cl-和Br-的还原性强弱,能证明结论的实验现象是______________________________________________________。
(5)若利用装置A、E进行乙烯与溴水反应的实验,写出反应的化学方程式________________________________________________________________。
(6)将装置B、C分别与F相连后,进行H2S与SO2反应的实验。F的烧瓶中发生反应的化学方程式为______________________;F的烧杯所起的作用是________________________________________________________________。
下面是某课外活动小组在进行探究乙醇性质实验时遇到的问题,请你帮忙解决。
在做乙醇与钠反应的实验时,把一小块钠缓慢放入装有乙醇的试管内,与钠与水反应相比有所不同:钠没有熔化成小球;钠先沉在试管底;反应后逐渐浮起。小组同学进行讨论,前两点现象解释达成共识。请说出你的看法。
(1)钠没有熔化成小球,因为_________。
(2)钠先沉在试管底,因为__________________。
(3)第三点现象解释存在争议,活动小组的同学形成两种意见:
a.生成的氢气产生浮力所致;
b.生成的乙醇钠增大了溶液的密度所致。
请你设计一个实验验证a和b说法的合理性。
)实验室制备硝基苯的方法是将苯与浓硫酸和浓硝酸的混合液加热到55~60 ℃反应,已知苯与硝基苯的基本物理性质如下表所示:
| 熔点 |
沸点 |
状态 |
|
| 苯 |
5.51 ℃ |
80.1 ℃ |
液体 |
| 硝基苯 |
5.7 ℃ |
210.9 ℃ |
液体 |
(1)要配制浓硫酸和浓硝酸的混合酸的注意事项是_________。
(2)分离硝基苯和水的混合物的方法是________;分离硝基苯和苯的方法是__________________________。
(3)某同学用如图装置制取硝基苯: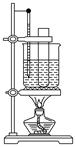
①用水浴加热的优点是_____________________;
②指出该装置的两处缺陷___________________;___________。
实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的二氧化硫。有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫。其装置如下图所示,试回答下列问题。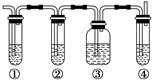
(1)图中①、②、③、④装置可盛放的试剂是
①________;②________;③________;④________。(将下列有关试剂的序号填入空格内)
| A.品红溶液 | B.NaOH溶液 |
| C.浓H2SO4 | D.酸性KMnO4溶液 |
(2)能说明二氧化硫气体存在的现象是________________________________。
(3)使用装置②的目的是________________________________。
使用装置③的目的是________________________________。
(4)能说明含有乙烯的现象是________________________________。
利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组通过在实验室中模拟上述过程,其设计的模拟装置如下: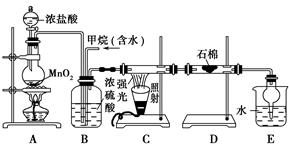
根据设计要求回答:
(1)B装置有三种功能:①控制气流速度;②均匀混合气体;③________。
(2)设V(Cl2)/V(CH4)=x,若理论上欲获得最多的氯化氢,则x值应________。
(3)D装置的石棉中均匀混有KI粉末,其作用是_____________________________________。
(4)E装置的作用是___________________(填编号)。
| A.收集气体 | B.吸收氯气 | C.防止倒吸 | D.吸收氯化氢 |
(5)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式________________________________。
(6)E装置除生成盐酸外,还含有有机物,从E中分离出有机物的最佳方法为________。该装置还有缺陷,原因是没有进行尾气处理,其尾气主要成分为________(填编号)。
a.CH4 b.CH3Cl c.CH2Cl2 d.CHCl3 e.CCl4
三苯甲醇( )是一种重要的化工原料和医药中间体,实验室合成三苯甲醇其合成流程如图1所示,装置如图2所示。
)是一种重要的化工原料和医药中间体,实验室合成三苯甲醇其合成流程如图1所示,装置如图2所示。
已知:(Ⅰ)格氏试剂容易水解, (碱式溴化镁);
(碱式溴化镁);
(Ⅱ)相关物质的物理性质如下:
| 物质 |
熔点 |
沸点 |
溶解性 |
| 三苯甲醇 |
164.2℃ |
380℃ |
不溶于水,溶于乙醇、乙醚等有机溶剂 |
| 乙醚 |
-116.3℃ |
34.6℃ |
微溶于水,溶于乙醇、苯等有机溶剂 |
| 溴苯 |
-30.7°C |
156.2°C |
不溶于水,溶于乙醇、乙醚等多数有机溶剂 |
| 苯甲酸乙酯 |
-34.6°C |
212.6°C |
不溶于水 |
| Mg(OH)Br |
常温下为固体 |
能溶于水,不溶于醇、醚等有机溶剂 |
(Ⅲ)三苯甲醇的分子量是260,纯净固体有机物一般都有固定熔点。
请回答以下问题:
(1)图2中玻璃仪器B的名称:;装有无水CaCl2的仪器A的作用是;
(2)图2中滴加液体未用普通分液漏斗而用滴液漏斗的作用是;制取格氏试剂时要保持微沸,可以采用(方式)加热,优点是;
(3)制得的三苯甲醇粗产品中,含有乙醚、溴苯、苯甲酸乙酯等有机物和碱式溴化镁等杂质,可以设计如下提纯方案,请填写如下空白:
其中,①操作为:;洗涤液最好选用:(从选项中选);
A、水 B、乙醚 C、乙醇 D、苯
检验产品已经洗涤干净的操作为:。
(4)纯度测定:称取2.60g产品,配成乙醚溶液,加入足量金属钠(乙醚与钠不会反应),充分反应后,测得生成气体体积为100.80ml标准状况)。产品中三苯甲醇质量分数为(保留两位有效数字)。