近年来,太湖蓝藻爆发,造成无锡市水质的严重恶化。这些事件再次敲响了我国水危机的警钟。在太湖流域某化工厂排放的污水中,常溶有某些对人体有害的物质,初步认为可能含有Fe3+、Ba2+、K+、OH-、Cl-、 、
、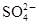 。为了进一步确认,取样进行实验检测:
。为了进一步确认,取样进行实验检测:
①取污水仔细观察,呈无色、透明、均一状态。
②向取样的污水中,滴入稀硫酸,有大量白色沉淀产生,再加稀硝酸,白色沉淀不消失。
③用pH试纸测定污水的pH,试纸显深蓝色。
(1)由此可知,该污水中肯定含有的离子是___________,肯定没有的离子是___________,可能含有的离子是___________。
(2)如何通过实验进一步确定溶液中可能存在的离子__________________________________。
绿原酸是一种新型高效的酚型天然抗氧化剂,在食品行业有着广泛的用途,在某些食品中可取代或部分取代目前常用的人工合成的抗氧化剂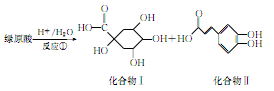
(1)化合物I的分子式为,反应①的反应类型为
(2)1 mol化合物I与足量金属钠反应生成标准状况下氢气的体积为
(3)写出化合物II与足量浓溴水反应的化学方程式
(4)1mol化合物II与足量的试剂X反应得到化合物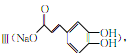 ,则试剂X是
,则试剂X是
(5)化合物IV有如下特点①与化合物II互为同分异构体;②遇 FeCl3溶液不显色;③1 mol化合物IV与足量银氨溶液反应生成4molAg;④1 mol化合物IV与足量NaOH溶液反应消耗4 mol NaOH;⑤核磁共振氢谱有4组峰,且峰面积之比为3:2:2:1,写出化合物IV所有可能的结构简式:
黄铜矿(CuFeS2)是制铜及其化合物的主要原料之一,还可以制备硫及铁的化合物。
(1)冶炼铜的反应为8CuFeS2+21O2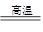 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是(填元素符号)。
(2)上述冶炼过程中产生大量SO2。下列处理方案合理的是(填代号)。
a.高空排放 b.用于制备硫酸
c.用纯碱溶液吸收制Na2SO3 d.用浓硫酸吸收
(3)过二硫酸钾(K2S2O8)具有强氧化性,可将I-氧化为I2:S2O82-+2I-=2SO42-+I2
通过改变反应途径,Fe3+可催化上述反应。试用离子方程式表示Fe3+对上述反应的催化过程。、
。
(不必配平,每空1分)。
(4)利用黄铜矿冶炼铜产生的炉渣(Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。方法为
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得。
据以上信息回答以下问题:选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液碘水
所选试剂为。证明炉渣中含有的实验现象为
。
从固体混合物A出发可以发生如下框图所示的一系列变化:
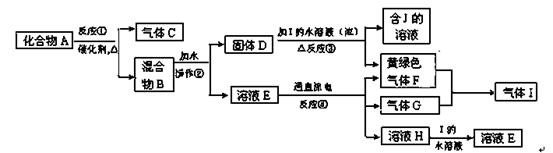
(1)在实验室中常用反应①制取气体C。若要收集气体C,可选择下图装置中的(填字母)
A B C
(2)操作②的名称是,在操作②中所使用的玻璃仪器的名称是。
(3)写出下列反应的方程式:
反应①的化学方程式
反应③的化学方程式
(4)在实验室中,要获得干燥纯净的黄绿色气体F, 可以将它通过下图中的装置,其中瓶I中盛放的
是,瓶II中盛放的是 。
已知A、B、C、D为常见单质,其中B、C、D常温常压下为气体,甲、乙、丙、丁为化合物,乙常温下为液体,丙的焰色反应为黄色,下图为各种物质之间的相互反应
(1)写出下列物质的化学式:
A,B,D,丙。
(2)丙电子式为,反应②中若有11.2L(标准状况下)B生成,则发生转移的电
子的物质的量为。
(3)写出反应③的化学方程式:
现有部分短周期元素的性质或原子结构如下表:
| 元素编号 |
元素性质或原子结构 |
| T |
单质能与水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子 |
| X |
最外层电子数是内层电子数的3倍 |
| Y |
第三周期元素的简单离子中半径最小 |
| Z |
T、X、Z组成的36电子的化合物A是家用消毒剂的主要成分 |
(1)元素T与X按原子个数比1:1形成的化合物B所含化学键为,该化合物的电子式为。
(2)化合物A的溶液呈碱性,用离子方程式解释其原因:,该化合物起消毒作用的微粒是。
(3)将Y与Z形成的化合物的水溶液逐滴加入到T的最高价氧化物对应水化物的溶液中直至过量(边滴边振荡),写出此过程中发生反应的离子方程式
、。