如图装置中,U形管内为红墨水,a、b试管中分别盛有食盐水和氯化铵溶液,各加入生铁块,放置一段时间。下列有关描述错误的是( )
| A.a中发生了吸氧腐蚀,b中发生了析氢腐蚀 |
| B.两试管中负极反应均是:Fe-2e-=Fe2+ |
| C.生铁块中碳作原电池正极 |
| D.在一段时间后,红墨水两边液面变为左低右高 |
如图装置中,U型管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液,各加入一生铁块,放置一段时间。下列有关描述错误的是


A.生铁块中的碳是原电池的正极 |
B.a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀 |
C.两试管中相同的电极反应式是:Fe-2e-= Fe2+ |
D.红墨水柱两边的液面变为左低右高 |
已知298K时,2SO2(g) + O2(g)  2SO3(g);△H =—Q1kJ/mol,在相同温度下,向密闭容器中通入4molSO2和1molO2,达到平衡时放出热量Q2 kJ,则下列关系式正确的是
2SO3(g);△H =—Q1kJ/mol,在相同温度下,向密闭容器中通入4molSO2和1molO2,达到平衡时放出热量Q2 kJ,则下列关系式正确的是
| A. Q2=2Q1 | B. Q2<2Q1 | C. Q2=Q1 | D.Q2<Q1 |
在下列给定条件下的溶液中,一定能大量共存的离子组是
| A.无色溶液中:Ca2+、H+、Cl-、HCO3-、MnO4- |
| B.能使pH试纸呈红色的溶液中:Na+、NH4+、NO3-、I- |
| C.FeCl3溶液中:K+、Na+、SO42-、AlO2- |
D.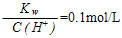 的溶液:Na+、K+、SiO32-、NO3- 的溶液:Na+、K+、SiO32-、NO3- |
在密闭容器中的一定量的混合气体发生反应:xA(g)+yB(g) zC(g),平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度为0.30mol/L。下列有关判断正确的是
zC(g),平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度为0.30mol/L。下列有关判断正确的是
| A.x+y<z | B.平衡向正反应方向移动 |
| C.B的转化率降低 | D.C的体积分数增大 |
在一定温度下,容器内某一反应中M、N的物质的量随反应时间的变化曲线如图,下列表述中不正确的是
A.反应的化学方程式为:2M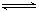 N N |
| B.t3时,正逆反应速率相等 |
| C.t2时,N的消耗速率大于N的生成速率 |
| D.t1时,N的浓度是M浓度的2倍 |