某研究性学习小组设计以下装置制取氯气,并以氯气为原料进行特定反应。分析并回答下列问题:
(1)装置A中,b 为电池的 (填“正”或“负”)极。
(2)实验开始时,先让氯气和水蒸气充满装有炭粉的装置C,再点燃C处的酒精灯,装置C中发生氧化还原反应,生成CO2和HCl(g),则反应的化学方程式为:
。
(3)要将装置B接入装置A和C之间,正确的连接顺序是:c→ → →f
(4)实验结束后,将装置B试管中的氯水倒入已检查完好的分液漏斗中,然后再注入10 mL CCl4,盖好玻璃塞,振荡,静置于铁架台上(如图)
等分层后取上层液和下层液,呈黄绿色的是 (填“上层液”或“下层液”),该层液体能否使干燥的有色布条褪色? (填“能”或“不能”)。
(5)若装置A中产生的氯气恰好能与100 mL 4 mol/L的NaOH溶液完全反应,则此时A中Pt电极(阴极)增加的质量为 g。
普利斯特里(Joseph Priestley)在拉瓦锡之前发现了氧气,但由于受“燃素说”的影响,他把氧气当作了“燃素”。拉瓦锡正是在普利斯特里研究的基础上,破除了“燃素说”的束缚,确认氧气是由一种元素形成的纯净物。普利斯特里在一次加热浓硫酸的实验中,由于不慎,造成了倒吸,将水槽中的水银(Hg)倒吸进加热后的浓硫酸中,并且烧坏了手。偶然中他发现热的浓H2SO4与水银发生了反应并生成了一种气体。这种气体就是由他发现的SO2。根据以上叙述判断下列说法不正确的是()
| A.浓H2SO4具有强腐蚀性,操作应格外小心 |
| B.为防止倒吸,实验结束时应先从水槽中取出导气管,后撤酒精灯 |
| C.实验中应仔细观察,不放过任何异常现象 |
| D.普利斯特里是一位失败的科学家,不值得尊敬 |
某同学在实验室发现两瓶白色固体,一瓶是硫酸钠,另一瓶是碳酸钠,但均已失去标签。下面是该同学检验这两瓶固体的方法,其中不能成功检验出硫酸钠和碳酸钠的是()
| A.分别取固体少许加入试管中,配成溶液,然后滴加氯化钡溶液 |
| B.分别取固体少许加入试管中,配成溶液,然后滴加氯化钡溶液,最后滴加盐酸 |
| C.分别取固体少许加入试管中,配成溶液,然后滴加盐酸,最后滴加氯化钡溶液 |
| D.分别取固体少许加入试管中,配成溶液,然后滴加盐酸酸化的氯化钡溶液 |
2006年6月1日讯中共中央政治局常委、国务院总理温家宝近日就2006年环保专项行动作出重要批示,部署2006年整治违法排污企业保障群众健康环保专项行动。水、大气、土壤等污染日益严重,重金属、有毒化学物质和持久性有机物等污染持续增加。一些地方已经喝不到干净的水,呼吸不到清洁的空气,土壤污染严重危及农产品安全。环境污染和生态破坏造成了巨大经济损失,严重危害群众健康,成为人民群众的切肤之痛。环境污染问题是举世瞩目的社会热点问题,下列收集气体的方法既能达到收集目的又符合环保要求的是()
A.用如图所示的方法收集二氧化硫(二氧化硫的密度比空气大)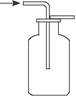 |
B.用下图所示的方法收集二氧化氮(已知:二氧化氮的密度比空气的密度大、有毒但能溶于氢氧化钠溶液)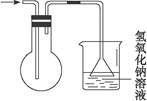 |
C.用右图所示的方法收集一氧化碳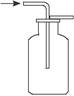 |
D.用右图所示的方法收集氢气 |
用18 mol·L-1浓硫酸配制100 mL 3.0 mol·L-1稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸③溶解 ④转移、洗涤 ⑤定容、摇匀
完成下列问题:
(1)所需浓硫酸的体积是________,量取浓硫酸所用的量筒的规格是________(从下列中选用A.10 mL B.25 mL C.50 mL D.100 mL)。
(2)第③步实验的操作是________________________________。
(3)第⑤步实验的操作是________________________________。
(4)下列情况对所配制的稀硫酸浓度有何影响?(用“偏大”“偏小”“无影响”填写)
A.所用的浓硫酸长时间放置在密封不好的容器中________________________________
B.容量瓶用蒸馏洗涤后残留有少量的水________________
C.所用过的烧杯、玻璃棒未洗涤________________
D.定容时俯视刻度线________________
欲配制100 mL 1.0 mol·L-1 Na2SO4溶液,正确的方法是( )
①将14.2 g Na2SO4溶于100 mL水中 ②将32.2 g Na2SO4·10H2O溶于少量水中,再用水稀释至100 mL ③将20 mL 5.0 mol·L-1 Na2SO4溶液用水稀释至100 mL
| A.①② |
| B.②③ |
| C.①③ |
| D.①②③ |