已知硫酸、氨水的密度与所加水量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
| |
溶质的物质的量 浓度/mol·L-1 |
溶液的密度 /g·cm-3 |
| 硫酸 |
c1 |
ρ1 |
| 氨水 |
c2 |
ρ2 |
(1)表中硫酸的质量分数为_____(不写单位,用含c1、ρ1的代数式表示)。
(2)物质的量浓度为c1 mol·L-1的硫酸与水等体积混合(混合后溶液体积变化忽略不计),所得溶液的物质的量浓度为_____mol·L-1。
(3)物质的量浓度为c2 mol·L-1的氨水与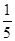 c2 mol·L-1的氨水等质量混合,所得溶液的密度_____ (填“大于”、“小于”或“等于”,下同)ρ2 g·cm-3,所得溶液的物质的量浓度_____
c2 mol·L-1的氨水等质量混合,所得溶液的密度_____ (填“大于”、“小于”或“等于”,下同)ρ2 g·cm-3,所得溶液的物质的量浓度_____ c2 mol·L-1(设混合后溶液的体积变化忽略不计)。
c2 mol·L-1(设混合后溶液的体积变化忽略不计)。
选考【化学——选修3:物质结构与性质】1967年舒尔滋提出金属互化物的概念,其定义为固相金属间化合物拥有两种或两种以上的金属元素,如Cu9Al4、Cu5Zn8等。回答下列问题:
(1)某种金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于____(填“晶体”或“非晶体”)。
(2)基态铜原子的核外电子排布式为____;在CuSO4溶液中滴入过量氨水,形成配合物的颜色为____。
(3)铜能与类卤素(SCN)2反应生成Cu(SCN)2,1mol(SCN)2分子中含有σ键的数目为________;卤素(SCN)2对应的酸有两种,理论推测硫氰酸(H—S—C≡N)的沸点低于异硫氰酸(H—N=C=S)的沸点,其原因是____。
(4)金属锌晶体的堆积方式为____。在ZnS晶胞中(结构如图1所示),S2-的配位数为____。
(5)铜有两种氧化物CuO、Cu2O,高温时易转化为Cu2O的原因为____(请从原子结构的角度解释)。
(6)铜与金形成的金属互化物结构如图2所示,其晶胞边长为apm,该金属互化物的密度为____g/cm3。(用含a、NA的代数式表示)
用辉铜矿(主要成分为 Cu2S,含少量Fe2O3、SiO2,等杂质)制备难溶于水的碱式碳酸铜的流程如下:
(1)下列措施是为了加快浸取速率,其中无法达到目的的是____(填字母)。
| A.延长浸取时间 | B.将辉铜矿粉碎 |
| C.充分搅拌 | D.适当增加硫酸浓度 |
(2)滤渣I巾的主要成分是MnO2、S、SiO2,请写出“浸取”反应中生成S的离子方程式:_______。
(3)研究发现,若先除铁再浸取,浸取速率明显变慢,可能的原因是___________。
(4)“除铁”的方法是通过调节溶液pH,使Fe3+转化为Fe(OH)3,则加入的试剂A可以是_______(填化学式);“赶氨”时,最适宜的操作方法是________。
(5)“沉锰”(除Mn2+)过程中有关反应的离子方程式为_______。
(6)滤液Ⅱ经蒸发结晶得到的盐主要是___________(填化学式)。
(16分)为治理环境,减少雾霾,应采取措施减少二氧化硫、氮氧化物(NOx)和CO2的排放量。
I.处理NOx的一种方法是利用甲烷催化还原NOx。
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=—574 kJ/mol
②CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H2=—867kJ/mol
(1)若用4.48LCH4还原NO生成N2,则放出的热量为______kJ。(气体体积已折算为标准状况下)
(2)NOx可用强碱溶液吸收产生硝酸盐。在酸性条件下,FeSO4溶液能将NO3-还原为NO,NO能与多余的FeSO4溶液作用生成棕色物质,这是检验NO3-的特征反应。电解的原理如图所示
则:写出该过程中产生NO的离子方程式:____________。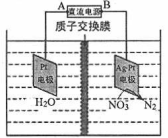
(3)电解时阴极的电极反应式为____;当电路中转移20 mol电子时,交换膜左侧溶液质量减少________g。
Ⅲ利用I2O5消除CO污染的反应为:5CO(g)+I2O5(s) 5CO2(g)+I2(s)。不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4 molCO,测得CO2的体积分数(
5CO2(g)+I2(s)。不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4 molCO,测得CO2的体积分数(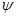 )随时间(t)变化曲线如图。
)随时间(t)变化曲线如图。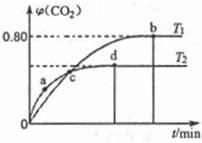
回答:
(4)T1时,该反应的化学平衡常数的数值为____。
(5)下列说法不正确的是_______(填字母)。
| A.容器内气体密度不变,表明反应达到平衡状态 |
| B.两种温度下,c点时体系中混合气体的压强相等 |
| C.d点时,在原容器中充入一定量氦气,CO的转化率不变 |
| D.b点和d点时化学平衡常数的大小关系:Kb<Kd |
Ⅳ.以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4通过反应CO2(g)+CH4(g) CH3COOH(g)△H<0直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。
CH3COOH(g)△H<0直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。
(6)①250—300℃时,乙酸的生成速率减小的主要原因是_______。
②工业生产中该反应的温度常选择250℃、不选择400℃,从综合经济效益考虑,其原因是_______。
选做(12分)【化学——物质结构与性质】第二周期中碳、氮、氧是构成生命物质的三种主要元素,其单质及化合物在生产生活中也有着重要的应用。
(1)第二周期中,元素的第一电离能处于B与N之间的元素有_________种。
(2)某元素位于第四周期VIII族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为_________________________。
(3)乙烯酮(CH2=C=O)是一种重要的有机中间体,可用CH3COOH在痕量(C2H5O)P=O存在下加热脱H2O得到。乙烯酮分子中碳原子杂化轨道类型是________。CH3COOH的沸点比HCOOCH3高的主要原因是_______________________。
(4)CH2=CHCN是制备晴纶的原料,其分子中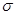 键和
键和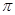 键的个数之比为______(填最简整数比)。
键的个数之比为______(填最简整数比)。
(5)碳化硅的结构与金刚石类似,其硬度仅次于金刚石,具有较强的耐磨性能。每个碳原子周围与其距离最近的硅原子有________个。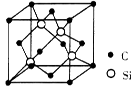
(17分)氮及其化合物在工业生产和科技等领域有广泛应用。
(1)肼(N2H4)常用于火箭或原电池的燃料。已知:(i)N2(g)+2O2(g)=2NO2(g) ΔH=+67.7kJ/mol
(ii)N2H4(g)+ O2(g)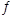 N2(g)+2H2O(g) ΔH=-534kJ/mol
N2(g)+2H2O(g) ΔH=-534kJ/mol
(iii)H2O(g)= H2O(1)ΔH=-44kJ/mol
①反应2N2H4(g)+2NO2(g)=3N2(g)+4H2O(l)ΔH =_______kJ·mol-1
②一定温度下,将N2H4与NO2以体积比1:1置于10 L密闭容器中发生反应2N2H4(g)+ 2NO2(g)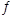 3N2(g)+4H2O(1),下列不能说明反应达到平衡状态的是_______。(填序号)
3N2(g)+4H2O(1),下列不能说明反应达到平衡状态的是_______。(填序号)
a.混合气体密度保持不变b.混合气体颜色保持不变
c.N2H4与NO2体积比保持不变 d.体系压强保持不变
③在10 L的密闭容器中发生上述反应,容器内部分物质的物质的量变化如下表:
前2min内NO2的平均反应速率为___________。平衡时NO2的转化率________;该温度下反应的平衡常数K=_________。
反应在第6min时改变了条件,改变的条件可能是__________。(填序号)
a.使用催化剂b.升高温度c.减小压强d.增加NO2的量
(2)HNO3和As2S3能发生反应:As2S3+10HNO3==2H3AsO4+3S+10NO2↑+2H2O,反应中被氧化的元素为_________。
若该反应中转移电子的物质的量为5 mol时,产物中的S经过转化全部生成浓H2SO4,然后与足量的铜在加热条件下反应消耗铜的量_________。(填序号)
a.小于0.75 molb.等于0.75mol c.大于0.75mold.无法确定