甲醇是一种重要的化工原料。甲醇与水蒸气催化重整可获得清洁能源,具有广泛的应用前景。现有如下实验,在体积为1 L的密闭容器中,充入1mol CH3OH和1molH2O,一定条件下发生反应:CH3OH (g)+ H2O (g) CO2(g) +3 H2 (g),测得CO2和CH3OH(g)的浓度随时间变化如下表所示。
CO2(g) +3 H2 (g),测得CO2和CH3OH(g)的浓度随时间变化如下表所示。
| 时间 物质 |
0 min |
10 min |
30 min |
60 min |
70 min |
| CO2(mol/L) |
0 |
0.2 |
0.6 |
0.8 |
0.8 |
| CH3OH(mol/L) |
1.0 |
0.8 |
0.4 |
0.2 |
0.2 |
①已知:CH3OH (g)+  O2 (g)
O2 (g) CO2(g) + 2H2 (g) H1= —192.9kJ/mol
CO2(g) + 2H2 (g) H1= —192.9kJ/mol
H2(g)+ O2 (g)
O2 (g) H2 O(g) H2= —120.9kJ/mol
H2 O(g) H2= —120.9kJ/mol
则甲醇与水蒸气催化重整反应的焓变△H3=_____ 。
②10~30 min内,氢气的平均反应速率v(H2)=___________mol/(L·min)。
③该反应的平衡常数表达式为K=__________________。
④下列措施中能使平衡时n(CH3OH)/n(CO2)减小的是(双选)___________。
A.加入催化剂 B.恒容充入He(g),使体系压强增大
C.将H2(g)从体系中分离 D.再充入1molH2O
(2)甲醇在催化剂条件下可以直接氧化成甲酸。
①在常温下,用0.1000 mol/L NaOH溶液滴定20. 00 mL 0.1000 mol/L 甲酸溶液过程中,当混合液的pH=7时,所消耗的V(NaOH)___(填“<”或“>”或“=”) 20. 00 mL。
②在上述滴定操作中,若将甲酸换成盐酸,请在图中的相应位置画出相应的滴定曲线。(1滴溶液约0.04mL) 
目前世界各国获得镁的主要来源 从海水中提取,以下是提取镁的过程中涉及到的几种物质常温下的溶度积常数,根据你所学的知识回答下面的几个问题:
从海水中提取,以下是提取镁的过程中涉及到的几种物质常温下的溶度积常数,根据你所学的知识回答下面的几个问题:
| 物质 |
CaCO3 |
MgCO3 |
Ca(OH)2 |
Mg(OH)2 |
| 溶度积 |
2.8×10-9 |
6.8×10-6 |
5.5×10-6 |
1.8×10-11 |
(1)在从海水中提取镁时,往往用到贝壳(主要成分是CaCO3),你认为(填“能”或“不能”)通过将贝壳研磨成粉末直接投入海水里制备含镁的沉淀,理由是。如果不能直接投入,应将贝壳作何处理,试写出化学方程式:。(若第一个空格填“能”,此空格不填;若填“不能”, 此空格只须第一步处理的化学反应方程式。)
(2)已知某地海水中的镁离子的浓度为1.8×10-3 mol·L-1,则常温下要使镁离子产生沉淀,溶液pH最低应为。
(3)实验室中常用CaCO3制CO2,其产物之一的氯化钙是应用广泛的化学试剂,可作干燥剂、冷冻剂等。为了测定某氯化钙样品中钙元素的含量,进行如下实验:
(I)准确称取氯化钙样品0.2000g,放入烧杯中,加入适量6mol/L的盐酸和适量蒸馏水使样品完全溶解,再加入35mL 0.25mol/L (NH4)2C2O4溶液,水浴加热,逐渐生成CaC2O4沉淀,经检验,Ca2+已沉淀完全。
(II)过滤并洗涤(I)所得沉淀。
(III)加入足量的10% H2SO4溶液和适量的蒸馏水,(II)中沉淀完全溶解,溶液呈酸性,加热至75℃,趁热逐滴加入0.05000 mol/L KMnO4溶液16.00mL,恰好完全反应。请回答:
已知滴定过程发生的反应为2MnO4- + 5H2C2O4 + 6H+ ="=2" Mn2+ +10 CO2↑+8 H2O(已配平)
①0.05000 mol/L KMnO4溶液标准溶液应置于(选填“酸式”或“碱式”)滴定管中。
②滴定终点的现象为。
③该氯化钙样品中钙元素的质量百分数为。
能源短缺是人类社会面临的重大问题,利用化学反应可实现多种形式的能量相互转化。请回答以下问题:
(1)由气态基态原子形成1mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是旧键断裂和新键的形成过程。已知反应N2(g)+3H2(g) 2NH3(g) △H=-93 kJ·mol-1。试根据表中所列键能数据,计算a 的数值为_______kJ/mol。
2NH3(g) △H=-93 kJ·mol-1。试根据表中所列键能数据,计算a 的数值为_______kJ/mol。
| 化学键 |
H-H |
N-H |
N≡N |
| 键能/kJ·mol-1 |
436 |
a |
945 |
(2)甲醇是一种可再生能源,具有广泛的开发和应用前景。已知在常压下有如下变化:
① 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH =a kJ/mol
② H2O(g)=H2O(l)ΔH =b kJ/mol
写出液态甲醇完全燃烧生成二氧化碳和液态水的热化学方程式:。
(3)可利用甲醇燃烧反应设计一个燃料电池。如下图1,用Pt作电极材料,用氢氧化钾溶液作电解质溶液,在两个电极上分别充入甲醇和氧气。
①写出燃料电池正极的电极反应式。②若利用该燃料电池提供电源,与图1右边烧杯相连,在铁件表面镀铜,则铁件应是极(填”A”或”B”);当铁件的质量增重6.4g时,燃料电池中消耗氧气的标准状况下体积为L。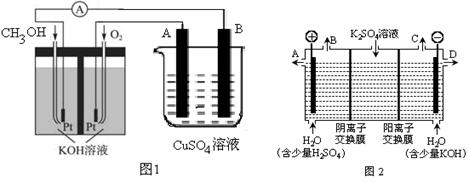
(4)如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图2装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾(电解槽内的阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过)。
①该电解槽的阳极反应式为,单位时间内通过阴离子交换膜的离子数与通过阳离子交换膜的离子数的比值为。
②从出口D导出的溶液是(填化学式)。
下表是中学化学教科书中元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答问题。
 |
IA |
0 |
|||||||
| 1 |
① |
II A |
III A |
IV A |
V A |
VI A |
VIIA |
||
| 2 |
② |
③ |
Ne |
||||||
| 3 |
④ |
⑤ |
Al |
S |
⑥ |
(1)⑥表示的元素是;
(2)②的原子结构示意图是;
(3)由①和③两种元素组成的化合物的化学式是;
(4)④和⑤两种元素的金属性强弱顺序是④ ⑤(填“<”或“>”)。
钠是活泼金属的代表,钠和钠的化合物是中学化学的基础知识。请回答下列有关问题。
(1)钠跟水剧烈反应,生成和氢气(H2),此实验说明钠的化学性质活泼;
(2)钠有两种氧化物,其中能用于呼吸面具和潜水艇中作为氧气来源的氧化物是:
;
(3)固体碳酸钠中含有碳酸氢钠杂质,除去此杂质的简单方法是(填“萃取”或“加热”或“蒸馏”)。
根据乙烯和乙醇的知识填空。
(1)完成下列化学方程式:CH2= CH2+ CH3CH2OH;
CH3CH2OH;
(2)乙醇跟乙酸在浓硫酸催化且加热的条件下反应,制取的是。