现有4种有机物:
| A.乙烯, | B.乙醇, | C.乙酸, | D.,.乙酸乙酯。 |
在上述4种有机物中(填写字母,每空只填一个字母):
①能发生水解反应的是 。
②具有酸性且能发生酯化反应的是 。
③既能发生加成反应,又能发生聚合反应的是 。
结构决定性质,性质体现结构。对结构和性质的研究是学好化学的基础。
(1)N、O、S三种元素的第一电离能大小顺序为:>>。(填元素符号)
(2)某晶体的晶胞如图所示,X位于体心,Y位于4个面心,Z位于8个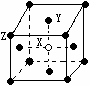 顶点,该晶体中 X、Y、Z的粒子个数比为______________;
顶点,该晶体中 X、Y、Z的粒子个数比为______________;
(3)按所示格式填写下表有序号的空格:
| 原子序数 |
原子价层电子排布 |
周期 |
族 |
| 17 |
① |
第三 |
② |
| ③ |
3d54s1 |
④ |
ⅥB |
(4)某元素的激发态原子的电子排布式为1s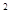 2s
2s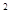 2p
2p 3s
3s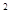 3p
3p 4s
4s ,则该元素的最高价氧化物对应的水化物的化学式是。
,则该元素的最高价氧化物对应的水化物的化学式是。
(5)NH4CuSO3中的金属阳离子的核外电子排布式为。
(1)在我国使用最早的合金是,目前用量最大,用途最广泛的合金是。
(2)0.5 mol H2O 的质量为g,共有个原子。
(3)质量都是50g 的Cl2、NH3、CO2、O2四种气体中,含有分子数最少的是;在相同的温度和压强下,体积最大的是。
(4)配制50mL 0.2mol/L CuSO4溶液,需要CuSO4•5H2O g。
(5)氯气可用于自来水的杀菌、消毒,请用化学方程式和简要的文字说明理由:
。
(共14分)右图中,A为空气中常见的气体单质、B、C、E是金属单质,D为非金属单质。已知:①I是一种常见的温室气体,E原子核内有12个质子②反应 能放出大量的热,该反应曾应用于铁轨的焊接;回答下列问题:
能放出大量的热,该反应曾应用于铁轨的焊接;回答下列问题: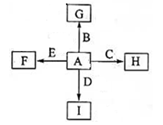
(1)分别写出F、G、H、I的化学式
F G H I
(2)书写下列化学方程式 ;
;
(3)C与NaOH溶液反应的化学方程式为,
反应后溶液与过量化合物I反应的化学方程式为;
⑷1.6gG溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需的铜粉的质量为:
(提示 :2FeCl3+ Cu ==2FeCl2+ CuCl2);
已知A经如下图所示的过程转化为D,,请回答下列问题:
(1)若A为非金属单质,且常温下为淡黄色固体,B为刺激性气味的无色气体,能使品红溶液褪色,D为强酸。
①D的化学式是。
②在工业生产中B气体的大量排放被雨水吸收后形成了而污染了环境。
③ D的浓溶液在加热下可与铜反应并生成B气体,请写出该反应的化学方程式
。指出该反应的氧化剂为 ,
还原产物为 反应中每生成1mol B气体,转移mol电子。
(2)若A为金属单质,C是淡黄色固体,D为强碱
①写出C→D的化学方程式
该反应(填“属于”、“不属于”)氧化还原反应。
若阿伏加德罗常数用NA表示,请回答下列问题:
(1).0.5 mol H2O的质量为 ,其中含有个水分子,共有个原子。
(2).现有mg某气体,它由双原子分子构成,它的摩尔质量为M g·mol-1,则:
①该气体的物质的量为________mol。
②该气体在标准状况下的体积为____________L。
③该气体溶于水后形成VL溶液(不考虑反应),其溶液的物质的量浓度为___mol·L-1。