镓(Ga)、锗(Ge)、砷(As)、硒(Se)均为第四周期的元素,它们在高科技尖端科学特别是信息领域有着广泛的用途。试回答下列问题:
(1)基态锗原子的价电子排布式为_________________________________。
(2)沸点:NH3________AsH3(填“>”、“<”或“=”,原因是_____________________。
(3)某砷的氧化物俗称“砒霜”,其分子结构如图所示,该化合物的分子式为_______,As原子采取__________杂化。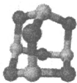
(4)H2SeO4和H2SeO3是硒的两种含氧酸,请根据结构与性质的关系,解释H2SeO4比H2SeO3酸性强的原因________________________。
(5)砷化镓可由(CH3)2Ga和AsH3在700℃下反应制得,反应的方程式为_________________;砷化镓的晶胞结构如下图所示,其晶胞边长为a pm,则每立方厘米该晶体中所含砷元素的质量为____________g(用NA表示阿伏加德罗常数的值)。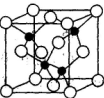
溴化碘(IBr)的化学性质类似于卤素单质,试回答下列问题:
(1)溴化碘的电子式是,它是由键形成的分子。(填极性或非极性)
(2)溴化碘和水反应生成了一种三原子分子,该分子的电子式为,
它的VSEPR模型是 ,分子构型是 。
有以下物质:①CH4,②C2H4,③H2O,④NH3,⑤CH2O,⑥CO2;
非极性分子的是______________;既有σ键又有π键的是__________;中心原子没有孤电子对的是______________;中心原子杂化类型为sp3的是;分子构型都是直线形的是。(写序号)
第四周期元素中,4p轨道半充满的是,3d轨道半充满的是,4s轨道半充满的是。(写元素符号)
已知某元素的原子序数是26,试推测:
(1)该元素的简化电子排布式为;
(2)该元素处在周期族;
(3)该元素的常见化合价是。
某同学取一定量的Al和Fe固体混合物,与2.0 L极稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4 mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。试回答下列问题: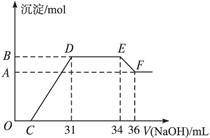
1、图中OC段没有沉淀生成,此阶段发生反应的离子方程式为。
在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为;上述现象说明溶液中______________结合OH-的能力比___________强(填写离子符号)。
2、B与A的差值为______________mol。
3、B点对应的沉淀的物质的量为____________mol,C点对应的氢氧化钠溶液的体积为______________mL。
4、求原硝酸溶液的物质的量浓度?