高锰酸钾在实验室和工农业生产中有广泛的用途.实验室以二氧化锰为主要原料制备高锰酸钾。其部分流程如下:
(1)第①步加热熔融应在 中进行.而不用瓷坩埚的原因是 (用化学程式表示)。
(2)第④步通入CO2,可以使Mn片发生反应.生成MnO4—和MnO2。反应的离子方程式为 。则完成反应时,转化为KMnO4的占全部K2MnO4的百分率约为 (精确到0.1%)。
(3)第⑤步趁热过滤的是 。
(4)第⑥步加热浓缩至液面有细小晶体析出时.停止加热.冷却结晶、 、洗涤、干燥。干燥过程中.温度不宜过高.其原因是 (用化学方程式表示)。
(5)H2O2和KMnO4,都是常用的强氧化剂。若向H2O2溶液中滴加酸性高锰酸钾溶液.则酸性高锰酸钾溶液会褪色.写出该反应的离子方程式: .该反应说明H2O2的氧化性比KMnO4 (填“强”或“弱”)。
用足量的CO还原14 g铁的氧化物的混合物,将生成的气体通入足量的澄清石灰水中,生成沉淀25 g,则这种混合物组成是①FeO、Fe2O3 ②FeO、Fe3O4 ③Fe2O3、Fe3O4中的 ,其物质的量之比为 。
(1)下列反应原理不符合工业冶炼金属实际情况的是( )。
A.2HgO 2Hg+O2↑ 2Hg+O2↑ |
B.Fe3O4+4CO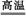 3Fe+4CO2 3Fe+4CO2 |
C.2MgO 2Mg+O2↑ 2Mg+O2↑ |
D.2Ag2O 4Ag+O2↑ 4Ag+O2↑ |
(2)简要说明不符合工业实际的原因: 。
有A、B、C、D四种元素,A和B两种元素的原子各有两个电子层;C、D两元素的原子各有三个电子层。A和B能化合生成无色无味的气体AB2,C和D能化合生成C2D,B和D是同族元素,B离子和C离子核外电子数相同。
(1)这四种元素分别是:A ,B ,C ,D 。
(2)用电子式表示C和D形成化合物的过程: 。
根据元素周期表1~20号元素的性质和递变规律,回答下列问题。
(1)属于金属元素的有 种,金属性最强的元素与氧气反应生成的化合物有 (填两种化合物的化学式)。
(2)属于稀有气体的是 (填元素符号,下同)。
(3)形成化合物种类最多的两种元素是 。
(4)第三周期中,原子半径最大的是(稀有气体除外) 。
(5)推测Si、N最简单氢化物的稳定性 大于 (填化学式)。
A、B、C、D 4种元素的原子序数均小于18,其最高正价依次为+1、+4、+5、+7,已知B的原子核外次外层电子数为2。A、C原子的核外次外层电子数为8。D元素的最高价氧化物对应水化物是已知无机含氧酸中最强的酸。则:
(1)A、B、C、D分别是 、 、 、
(2)A的离子结构示意图为 ,C的原子结构示意图为
(3)C的最高价氧化物对应水化物与A的氢氧化物反应生成 种盐,其化学式为 、 、 (可不填满,也可补充)
(4)C、D的气态氢化物稳定性由强到弱的顺序是