X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
| 元素 |
相关信息 |
| X |
X的最高价氧化物对应的水化物化学式为H2XO3 |
| Y |
Y是地壳中含量最高的元素 |
| Z |
Z的基态原子最外层电子排布式为3s23p1 |
| W |
W的一种核素的质量数为28,中子数为14 |
(1)W位于元素周期表第________周期第________族;W的原子半径比X的________(填“大”或“小”)。
(2)Z的第一电离能比W的________(填“大”或“小”);XY2由固态变为气态所需克服的微粒间作用力是________;氢元素、X、Y的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称________。
(3)振荡下,向Z单质与盐酸反应后的无色溶液中滴加NaOH溶液直至过量,能观察到的现象是________;W的单质与氢氟酸反应生成两种无色气体,该反应的化学方程式是_________________________________________________。
有一瓶无色澄清的溶液,其中可能含Na+、Mg2+、H+、Fe3+、CO32-、Cl-、Br-中的一种或几种,取该溶液进行如下实验:
①用PH试纸检验,表明溶液呈强酸性
②取部分溶液,加入少量的CCl4及数滴新制的氯水,振荡后CCl4层显橙红色
③将②得到的溶液滴加硝酸银溶液,有白色沉淀生成,滴加稀硝酸沉淀不溶解。
④另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成
根据上述实验事实确定并回答:
(1)在溶液中,肯定存在的离子有。
(2)肯定不存在的离子有。
(3)可能存在的离子有。
新制氯水中含有多种粒子,某校化学研究性学习小组的同学为探究其组成,做了如下实验,回答:
(1)往用水湿润的红纸中滴入少量新制饱和氯水,观察到现象,说明饱
和氯水中含有。
(2)在试管中加入少量的块状碳酸钙,再加入适量饱和氯水,充分反应,有少量气泡产
生,用离子方程式解释此现象。
加入0.1 mol的MnO2粉末于50 mL过氧化氢的溶液中(密度为1.1 g·mL-1),在标准状况下放出气体的体积和时间的关系如图所示,回答下列问题。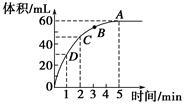
(1)A、B、C、D四点化学反应速率快慢的顺序为____________________。
(2)解释反应速率变化的原因__________________________________。
(3)计算过氧化氢的初始物质的量浓度________。
(4)求反应进行到2分钟时过氧化氢的质量分数。
在下列事实中,什么因素影响了化学反应的速率?
(1)集气瓶中有H2和Cl2的混合气体,在瓶外点燃镁条时发生爆炸________;
(2)黄铁矿煅烧时要粉碎成细小的矿粒________;
(3)KI晶体和HgCl2晶体混合后无明显现象,若一起投入水中,很快生成红色HgI2___________________________;
(4)熔化的KClO3放出气泡很慢,撒入少量MnO2后很快产生气体________;
(5)同浓度、同体积的盐酸中放入同样大小的锌粒和镁块,产生气体的速率有快有慢________;
(6)同样大小的石灰石分别在0.1 mol·L-1的盐酸和1 mol·L-1的盐酸中反应速率不同________;
(7)夏天的食品易变霉,冬天就不易发生该现象__________________________________
(8)葡萄糖在空气中燃烧时需要较高的温度,可是在人体里,在正常体温(37 ℃)时,就可以被氧化,这是因为______________________________________________
反应A+3B=2C+2D在四种不同情况下的反应速率可分别为
①v
| A.=0.15 mol/(L·s) ②v | B.=0.6 mol/(L·s) ③v | C.=0.4 mol/(L·s) ④v | D.=0.45 mol/(L·s) |
该反应进行的快慢顺序为________。