卤素性质活泼,能形成卤化物、多卤化物等多种类型的化合物。
(1)卤化氢中,HF的沸点高于HCl,原因是____________________________
____________________________________________。
(2)如图为F-与Mg2+、K+形成的某种离子晶体的晶胞,其中“○”表示的离子是________(填离子符号)。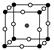
(3)多卤化物Rb[ICl2]分解时生成晶格能相对较大的铷(Rb)的卤化物,则该卤化物的化学式为_______________。
(4)BF3与NH3能发生反应生成X(H3BNF3),X的结构式为____________(用“→”表示出配位键):X中B原子的杂化方式为____________________________。
(5)有一类物质的性质与卤素类似,称为“拟卤素”[如(SCN)2、(CN)2等]。(CN)2的结构式为CNCN,该分子中σ键和π键数目之比为________。
(12分)某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中的溶质足量),当闭合该装置的电键K时,观察到电流表的指针发生了偏转。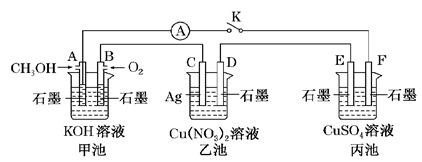
请回答下列问题:
(1)甲池为________(填“原电池”、“电解池”或“电镀池”),A电极的电极反应式为_____________。
(2)丙池中F电极为________(填“正极”、“负极”、“阴极”或“阳极”),该池的总反应方程式为____________________________________________________________。
(3)当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为________mL(标准状况)。
(4)一段时间后,断开电键K。下列物质能使乙池恢复到反应前浓度的是________(填字母)。
| A.Cu | B.CuO | C.Cu(OH)2 | D.Cu2(OH)2CO3 |
2SO2(g)+ O2(g) 2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH =" -" 99 kJ·mol-1
2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH =" -" 99 kJ·mol-1
请回答下列问题:
(1)图中A表示_____________________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________。
(2)图中ΔH =" __________" kJ·mol-1。
(3)如果反应速率v(SO2)为0.06 mol·L-1·min-1,则v(O2)为__________ mol·L-1·min-1。
(4)已知S(s) + O2(g) = SO2(g) ΔH =" -" 296 kJ·mol-1,则由S(s)生成5 mol SO3(g)的ΔH=kJ·mol-1。
已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下
3Cu + 8HNO3 ="=" 3Cu(NO3)2 + 2NO↑+ 4H2O
(1)用双线桥法分析上述反应(只需标出电子得失的方向和数目)
3Cu + 8HNO3 ="=" 3Cu(NO3)2 + 2NO↑+ 4H2O
(2)上述反应中氧化剂是,氧化产物是(填化学式)。
(3)若19.2g铜与足量硝酸完全反应,则消耗硝酸为mol,被还原的硝酸为mol,生成NO的体积为L(标准状况) 。
(11分)有五瓶损坏标签的试剂,分别盛有AgNO3溶液、稀硝酸、盐酸、氯化钡溶液、碳酸钾溶液,为了确定各瓶中是什么试剂,将它们任意编号为A、B、C、D、E,用小试管各盛少量多次进行两两混合反应,反应现象为:A与B、A与E产生沉淀,B与D、B与E产生沉淀,C与E、D与E产生气体,而C与D无反应现象。
由此,可判定各试剂瓶中所盛试剂为(写化学式)
A____________、B____________、C、____________、D____________、E____________。
另外,请写出下面要求的离子方程式:
(1)A与E:_______________________________________________________________。
(2)B与E:_______________________________________________________________。
(3)C与E:____________________________________________________________。
用单线桥表示下列反应
(1)2KClO3==2KCl+3O2↑(2)Zn+H2SO4==ZnSO4+H2↑