一定温度下,容积为2 L的甲、乙两固定容积的密闭容器中,发生反应:2SO2(g)+O2(g)  2SO3(g)。达平衡时测得有关数据如下表。
2SO3(g)。达平衡时测得有关数据如下表。
| 容器 |
甲 |
乙 |
| 反应物投入量 |
2 mol SO2、1 mol O2 |
4 mol SO3 |
| n(SO3)/mol |
1.6 |
a |
| 反应物的转化率 |
α1 |
α2 |
下列说法正确的是( )。
A.α1+α2>1
B.1.6<a<3.2
C.若甲中反应2 min时达到平衡,则2 min 内平均速率v(O2)=0.2 mol·L-1·min-1
D.甲平衡后再加入0.2 mol SO2、0.2 mol O2和0.4 mol SO3,平衡正向移动
已知在某密闭容器中发生反应 4NH3+5O2=4NO+6H2O,若反应速率分别用υ(NH3)、υ(O2)、υ(NO)、υ(H2O)表示,则下列关系正确的是
A.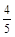 υ(NH3) =υ(O2) υ(NH3) =υ(O2) |
B.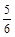 υ(O2) =υ(H2O) υ(O2) =υ(H2O) |
C.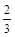 υ(NH3) =υ(H2O) υ(NH3) =υ(H2O) |
D.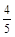 υ(O2) =υ(NO) υ(O2) =υ(NO) |
下列关于原电池、电解池的叙述中正确的是
| A.发生氧化反应的电极分别为负极和阴极 |
| B.阴离子分别向负极和阴极迁移 |
| C.电子流向分别由负极直接流向正极、阴极直接流向阳极 |
| D.若都有一个电极质量减轻,应分别为负极和阳极 |
下列说法正确的是
| A.放热反应一定能自发进行,吸热反应一定不能自发进行 |
| B.化学反应的反应热不仅与体系的始态和终态有关,也与反应的途径有关 |
| C.催化剂不仅能加快反应速率,也能增大反应物的转化率 |
| D.升高温度,能提高活化分子百分数,不能提高反应所需的活化能 |
下列溶液一定呈酸性的是
| A.pH<7的溶液 | B.c(H+)>c(OH—) 的溶液 |
| C.pH>7的溶液 | D.c(H+)<c(OH—) 的溶液 |
“每天一个苹果,医生远离我”,说明苹果对人体健康非常有益,苹果为人体提供的主要营养素是
| A.油脂 | B.无机盐 | C.蛋白质 | D.维生素 |