甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应来制备甲醇。
Ⅰ:CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=206.0 kJ·mol-1
Ⅱ:CO(g)+2H2(g)=CH3OH(g) ΔH=-129.0 kJ·mol-1
(1)CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为______________________________________________________。
(2)将1.0 mol CH4和2.0 mol H2O(g)通入容积为100 L的反应室,在一定条件下发生反应Ⅰ,测得在一定的压强下CH4的转化率与温度的关系如右图。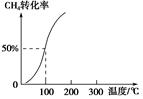
①假设100 ℃时达到平衡所需的时间为5 min,则用H2表示该反应的平均反应速率为________。
②100 ℃时反应Ⅰ的平衡常数为________。
(3)在压强为0.1 MPa、温度为300 ℃条件下,将a mol CO与3a mol H2的混合气体在催化剂作用下发生反应Ⅱ生成甲醇,平衡后将容器的容积压缩到原来的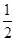 ,其他条件不变,对平衡体系产生的影响是________(填字母序号)。
,其他条件不变,对平衡体系产生的影响是________(填字母序号)。
| A.c(H2)减少 |
| B.正反应速率加快,逆反应速率减慢 |
| C.CH3OH 的物质的量增加 |
| D.重新平衡c(H2)/c(CH3OH)减小 |
E.平衡常数K增大
(4)写出甲醇-空气-KOH溶液的燃料电池负极的电极反应式:__________________________________________________。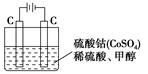
(5)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化。实验室用如图装置模拟上述过程:
①写出阳极电极反应式____________________________。
②写出除去甲醇的离子方程式__________________________________。
(每空2分,共10分)物质F是合成多种手性药物和生物活性物质的重要中间体,其合成路线如下: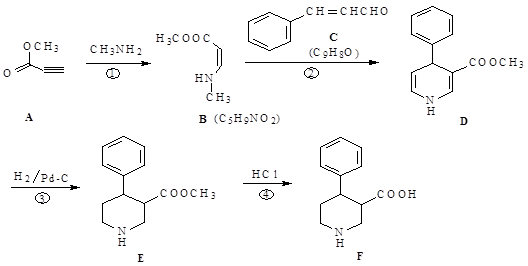
(1)反应①的类型为,反应④的类型为。
(2)物质A聚合可得聚丙炔酸甲酯,其结构简式为。
(3)物质C的俗名为肉桂醛,写出其同时满足下列条件的一种同分异构体的结构简式。
①能与氯化铁溶液显紫色;②苯环上有两个取代基;③分子的核磁共振氢谱有4个峰。
(4)若部分C被氧化为肉桂酸,反应②将产生副产物(分子式为C14H15NO3),写出其结构简式。
(每空1分,共8分)
由丙烯经下列反应可得到F和高分子化合物G,它们都是常用的塑料
请回答下列问题:
(1)F的同分异构体有很多,其中属于芳香烃(除去F自身外)有种,化合物E的官能团的名称:、。
(2)写出下列反应过程的反应类型:A→B:、E→G。
(3)写出B→C反应的化学方程式为。
(4)若A在NaOH的醇溶液反应,生成物仍为卤代烃,且其结构存在顺反异构,那么,A所发生的反应的化学方程式为。
(5)E的一种同分异构体M具有如下性质:①能发生银镜反应;②1mol M与足量的金属钠反应可产生1mol H2,则M的结构简式为_________ ____。(注:两个羟基连在同一碳上的结构不稳定)
(每空2分,共14分)A、B、C、D均为含苯环的化合物,且相对分子质量B>A>C,已知有机物A的结构简式为:
(1)A既能和NaOH溶液反应,又能和NaHCO3溶液反应,写出A和 NaHCO3溶液反应的化学方程式________________。
(2)①有机物B在浓硫酸存在条件下,相互作用生成一种环状酯(如下图)则有机物B的结构简式为_。
②等物质的量B与Na、NaOH、NaHCO3充分反应,消耗Na、NaOH、NaHCO3的物质的量之比为________。
(3) 1molA、C完全燃烧,消耗O2的质量相等,且1molC能和1molNa完全反应,写出含碳原子数最少的C的结构简式________,写出C与浓溴水的反应的化学方程式。
(4)D和B互为同分异构体,且知其苯环上连有三个取代基,苯环上的一氯代物只有两种,D不与NaHCO3溶液反应,能与Na和NaOH反应,等质量的D消耗Na和NaOH的物质的量之比为2∶3,则D的结构简式为、。(只写二种)
(每空2分,共8分)分子式为C3H6O3的物质有多种同分异构体,请写出符合下列要求的各种同分异构体的结构简式:(均用结构简式完成)
(1)A能与NaHCO3溶液反应,且1 molA与足量金属Na能生成1 molH2,则
A为或。
(2)B中所有同类原子的化学环境等同(如CH4中所有H所处化学环境等同),且不与Na反应,则B为。
(3)C中碳与氧分别有两种化学环境,氢的环境等同,且C与Na不反应,则C为。
(8分)X、Y、Z、W为按原子序数由小到大排列的四种短周期元素。
已知:①X可分别与Y、W形成X2Y、X2Y2、XW等共价化合物;②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物。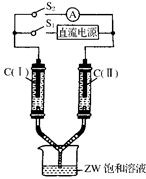
请回答:
(1)Z2Y的化学式是________________________。
(2)Z2Y2与X2Y反应的化学方程式是_______________________________________
(3)如图所示装置,两玻璃管中盛满滴有酚酞溶液的ZW饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。接通S1后,C(Ⅰ)附近溶液变红,两玻璃管中有气体生成。一段时间后(两玻璃管中液面未脱离电极),断开S1,接通S2,电流表的指针发生偏转。此时:
C(Ⅰ)的电极名称是________(填写“正极”或“负极”);
C(Ⅱ)的电极反应式是________________________________。
(4)铜屑放入稀硫酸不发生反应,若在稀硫酸中加入X2Y2,铜屑可逐渐溶解,该反应的离子方程式是____________________________________。