部分弱酸的电离平衡常数如下表:
| 弱酸 |
HCOOH |
HCN |
H2CO3 |
| 电离平衡 常数(25℃) |
Ki=1.77×10-4 |
Ki=4.9×10-10 |
Ki1=4.3×10-7 Ki2=5.6×10-11 |
下列选项正确的是( )。
A.2CN-+H2O+CO2=2HCN+CO32-
B.2HCOOH+CO32-=2HCOO-+H2O+CO2↑
C.等浓度的HCOONa和NaCN溶液的pH前者大于后者
D.中和等浓度的HCOOH和HCN消耗NaOH的量前者等于后者
下列说法中,不正确的是
| A.明矾和漂白粉均可用于自来水的杀菌、消毒 |
| B.光导纤维的主要成分是SiO2 |
| C.玻璃和陶瓷都属于传统硅酸盐材料 |
| D.大量排放SO2会引起酸雨 |
大胆科学的假设与猜想是科学探究的先导和价值所在。在下列假设(猜想)引导下的探究肯定没有意义的是
| A.探究SO2与Na2O2反应可能有Na2SO4生成 |
| B.探究Na与水的反应可能生成NaOH和H2O2 |
| C.探究浓H2SO4与铜在一定条件下反应产生的黑色物质中可能有CuS |
| D.探究向滴有酚酞试液的NaOH溶液中通以Cl2,酚酞红色褪去的现象是溶液的酸碱性变化所致,还是HClO的漂白性 |
高铁酸钠(Na2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强、无二次污染的绿色水处理剂。工业制高铁酸钠的方法有如下两种:
湿法制备的主要离子反应为:2Fe(OH)3 +3ClO-+4OH- = 2FeO42-+3Cl-+5H2O ,
干法制备的主要反应方程为:2FeSO4 +6Na2O2 = 2Na2FeO4 +2Na2O +2Na2SO4 +O2↑
则下列有关说法不正确的是
| A.高铁酸钠中铁显+6价 |
| B.湿法中FeO42—是氧化产物 |
| C.干法中每生成1mol Na2FeO4转移4mol电子 |
| D.K2FeO4可氧化水中的H2S、NH3,生成的Fe(OH)3胶体还能吸附悬浮杂质 |
下列离子在溶液中能大量共存,加入(NH4)2Fe(SO4)2•6H2O晶体后,仍能大量共存的是
| A.Na+、H+、Cl-、NO3- | B.Na+、Mg2+、Cl-、SO42- |
| C.K+、Ba2+、OH-、I- | D.Cu2+、CO32-、Br-、ClO- |
下列离子方程式与所述事实相符且正确的是
| A.氯气与水反应:Cl2+H2O=2H++Cl-+ClO- |
B.用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-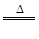 Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O |
| C.用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O |
| D.Fe3O4与稀HNO3反应:Fe3O4+8H+ =Fe2++2Fe3++4H2O |