偶氮苯是橙红色晶体,溶于乙醇,微溶于水,广泛应用于染料制造和橡胶工业,以硝基苯、镁粉和甲醇为原料制备偶氮苯的实验步骤如下:
步骤1:在反应器中加入一定量的硝基苯、甲醇和一小粒碘,装上冷凝管,加入少量镁粉,立即发生反应。
步骤2:等大部分镁粉反应完全后,再加入镁粉,反应继续进行,等镁粉完全反应后,加热回流30 min。
步骤3:将所得液体趁热倒入冰水中,并不断搅拌,用冰醋酸小心中和至pH为4~5,析出橙红色固体,过滤,用少量冰水洗涤。
步骤4:用95%的乙醇重结晶。
(1)步骤1中反应不需要加热就能剧烈进行,原因是________________。镁粉分两次加入而不是一次性全部加入的原因是___________________ _____________________________________________________。
(2)步骤3中析出固体用冰水洗涤的原因是________________。若要回收甲醇,实验所需的玻璃仪器除冷凝管、酒精灯、牛角管(应接管)和锥形瓶外还应有________________________________________________________________。
(3)取0.1 g偶氮苯,溶于5 mL左右的苯中,将溶液分成两等份,分别装于两个试管中,其中一个试管用黑纸包好放在阴暗处,另一个则放在阳光下照射。用毛细管各取上述两试管中的溶液点在距离滤纸条末端1 cm处,再将滤纸条末端浸入装有1∶3的苯环己烷溶液的容器中,实验操作及现象如下图所示:
①实验中分离物质所采用的方法是________法。
②由实验结果可知:________________;利用该方法可以提纯反式偶氮苯。
某学生实验小组,用稀硫酸和稀氢氧化钠溶液在下图所示的装置中,进行中和反应反应热的测定。请回答下列问题:
(1)图中装置缺少一种仪器,该仪器名称为__。
(2)写出该反应的热化学方程式(中和热为57.3kJ·mol-1):__________________。
(3)如果用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值将__________(填“偏大”、“偏小”或“无影响”)。
实验室用下图装置制取少量溴苯,试填写下列空白。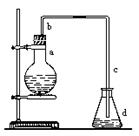
(1)在烧瓶a中装的试剂是铁粉、和。(各1分)
(2)请你推测长直导管b的作用:__________
(3)请你分析导管c的下口可否浸没于液面中?为什么? __________
(4)反应完毕后,向锥形瓶d中滴加AgNO3溶液有生成,此现象说明这种获得溴苯的反应属于:。(填有机反应类型)(各1分)
下图为某化学兴趣小组设计的乙醇氧化的实验装置(图中加热仪器、铁架台、铁夹等均未画出)。图中:A为无水乙醇(沸点为78℃),B为绕成螺旋状的细铜丝或银丝,C为无水CuSO4粉末,D为碱石灰,F为新制的碱性Cu(OH)2悬浊液。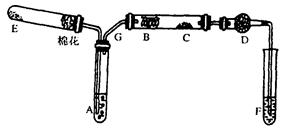
请回答下列问题:
(1)如图所示连接好装置后,在加入试剂之前,应先____。(操作名称)
(2)在上述装置中,实验时需要加热的仪器为(填仪器或某部位的代号)。
为使A中乙醇平缓均匀的气化成乙醇蒸气,常采用的操作方法是。
(3)图中D处使用碱石灰的作用是。
(4)C处观察到的现象是,F中观察到的现象是,说明B处发生的反应方程式是。
化学实验有助于理解化学知识,提升科学素养。某学习小组在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关探究。
(1)已知发生装置如图所示。请写出该反应的离子方程式。
制备实验开始时,先检查装置气密性,接下来的操作依次是(填序号)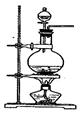
A.往烧瓶中加入MnO2粉末
B.加热
C.往烧瓶中加入浓盐酸
(2)为了制取纯净干燥的氯气,应将氯气依次通过盛有,的试剂瓶(填试剂名称)
(3)该小组关于实验中可制得氯气体积(标准状况)的讨论正确的是。
A.若提供0.4 mol HCl,MnO2不足量,则可制得氯气2.24 L
B.若提供0.4 mol HCl,MnO2过量,则可制得氯气2.24 L
C.若有0.4 mol HCl参与反应,则可制得氯气2.24 L
D.若有0.4 mol HCl被氧化,则可制得氯气2.24 L
(4)写出工业制氯气的化学方程式
实验室里用下列药品和仪器来制取纯净的无水氯化铜: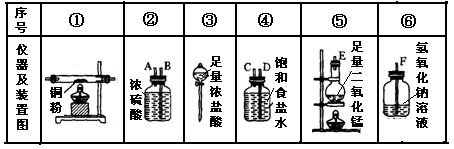
图中A、B、C、D、E、F的虚线部分表示玻璃管接口,接口的弯曲和伸长等部分未画出。根据要求填写下列各小题空白。
(1)如果所制得气体从左向右流向时,上述各仪器装置的正确连接顺序是(填各装置的序号)
接接接接接;
其中,②与④装置相连时,玻璃管接口(用装置中字母表示)应是接。
(2)装置⑥中发生反应的离子方程式是。
(3)实验开始时,应首先检验装置的;实验结束时,应先熄灭处的酒精灯。
(4)在装置⑤的烧杯中,发生反应的化学方程式为。
(5)待充分反应后,装置①的玻璃管中呈色。冷却后,将制得的产物配成溶液,溶液呈色。
(6)若反应中有71gCl2生成,则被氧化的HCl的物质的量为,转移电子数为。