制备无水乙醇的实验原理:由于乙醇95.6%、水4.4%组成一种混合物,常压下,它有一定的沸点(78.17 ℃),这个沸点低于水的(100 ℃)也低于纯乙醇的沸点(78.3 ℃),所以只靠简单蒸馏酒精,所得乙醇纯度最高只能达到95.6%,尚含有4.4%的水。如果要得到含量较高的乙醇,在实验室中常用的简便方法是加入生石灰回流(回流是在一个可以加热的反应容器中,把液体加热使受热转化生成的蒸气通过冷凝器冷凝又回流到原容器的操作。见图甲),回流之后再蒸馏,可得99.5%的乙醇,通常称为无水乙醇。如果要得到纯度更高的绝对乙醇(含乙醇99.95%),则还要用金属钠进行处理,借以除去最后微量的水分。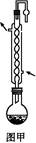
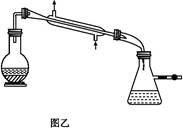
实验步骤:取干燥的250 mL圆底烧瓶一个,加入95%乙醇100 mL和小块生石灰30 g,振摇后用橡皮塞塞紧,放置过夜。在烧瓶口装上回流冷凝管,管口接一支氯化钙干燥管(装置见图甲),在水浴上加热回流1至2小时,稍冷,取下冷凝管,改装成蒸馏装置(如图乙),再放在热水浴中蒸馏,把最初蒸出的5 mL馏出液另外回收,然后用烘干的吸滤瓶作为接收器,其侧管接一支氯化钙干燥管,使其与大气相通,蒸至无液滴出来为止,量取所得乙醇的体积,计算回收率。请回答:
(1)为什么回收或蒸馏时都要装上氯化钙干燥管?
。
(2)为了防止回流系统外部湿气侵入,有人用塞子把冷凝管上端塞紧,这样做是否可行,为什么? 。
(3)无水氯化钙常用作吸水剂,如用无水氯化钙代替氧化钙投入酒精中,放置过夜,然后过滤。用此方法进行本实验制取乙醇是否可行,为什么?
。
(4)一般用干燥剂干燥有机物时,在蒸馏前应先过滤,但用氧化钙制备无水乙醇时,为什么可不过滤,留在瓶中一起蒸馏?
。
(5)为什么最初蒸出的5 mL馏出液另外收集,它的纯度是否已达99.5%?
。
纳米
在涂料、光催化、化妆品等领域有着极其广泛的应用。
制备纳米
的方法之一是
水解生成
,经过滤、水洗除去其中的
,再烘干、焙烧除去水分得到粉体
。
用现代分析仪器测定
粒子的大小。用氧化还原滴定法测定
的质量分数:一定条件下,将
溶解并还原为
,再以
溶液作指示剂,用
标准溶液滴定
至全部生成
。
请回答下列问题:
⑴
水解生成
的化学方程式为。
⑵ 检验
中
是否被除净的方法是。
⑶ 下列可用于测定
粒子大小的方法是(填字母代号)。
a.核磁共振法 b.红外 光谱法 c.质谱法 d.透射电子显微镜法
光谱法 c.质谱法 d.透射电子显微镜法
⑷ 配制
标准溶液时,加入一定量
的原因是;使用的仪器除天平、药匙、玻璃棒、烧杯、量简外,还需要下图中的 (填字母代号)。
(填字母代号)。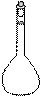


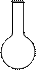
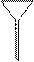
a b c d e
⑸ 滴定终点的现象是。
⑹ 滴定分析时,称取
摩尔质量为
)试样
,消耗
标准溶液
,则
质量分数表达式为。
⑺ 判断下列操作对
质量分数测定结果的影响(填"偏高"、"偏低"或"无影响")
① 若在配制标准溶液过程中,烧杯中的
溶液有少量溅出,使测定结果
② 若在滴定终点读取滴定管刻度时,俯视标准液液面,使测定结果。
请设计
在高温下与木炭反应生成
的实验。
(1)在下面方框中,
表示有长颈漏斗和锥形瓶组成的气体发生器,请在答题卡上的
后完成该反应的实验装置示意图(夹持装置,连接胶 管及尾气处理部分不必画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母
……;其他可选用的仪器(数量不限)简易表示如下:
管及尾气处理部分不必画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母
……;其他可选用的仪器(数量不限)简易表示如下:
(2)根据方框中的装置图,在答题卡上填写该表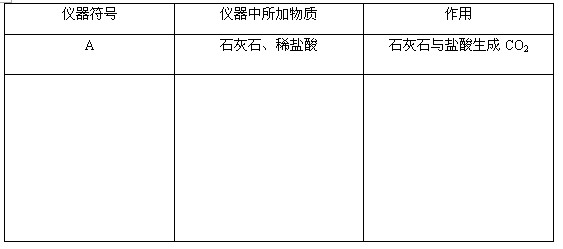
(3)有人对气体发生器作如下改进:在锥形瓶中放入一小试管,将长颈漏斗下端插入小试管中。改进后的优点是;
(4)验证
的方法是
请设计CO2在高温下与木炭反应生成CO的实验。
(1)在下面方框中,A表示有长颈漏斗和锥形瓶组成的气体发生器,请在答题卡上的A后完成该反应的实验装置示意图(夹持装置,连接胶 管及尾气处理部分不必画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母B、C……;其他可选用的仪器(数量不限)简易表示如下:
管及尾气处理部分不必画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母B、C……;其他可选用的仪器(数量不限)简易表示如下: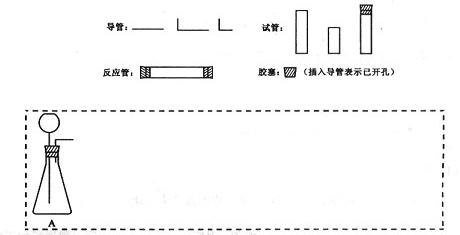
(2)根据方框中的装置图,在答题卡上填写该表
| 仪器符号 |
仪器中所加物质 |
作用 |
| A |
石灰石、稀盐酸 |
石灰石与盐酸生成CO2 |
(3)有人对气体发生器作如下改进:在锥形瓶中放入一小试管,将长颈漏斗下端插入小试管中。改进后的优点是________________________;
(4)验证CO的方法是____________________________;
以下是有关SO2、Cl2的性质实验。
(1)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质。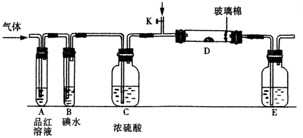
①若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同?(填“相同”或“不相同”);若置D装的是铁粉,通入Cl2与铁粉充分反应时现象为
;若装置D中装的是五氧化二钒(催化剂)。通入SO2时,打开K通入适量O2的化学反应方程式为。
②若装置B中装有5.0 mL 1.0×10-3mol/L在碘水,当通入足量Cl2完全反应后,共转移了5.0×10-5mol电子,该反应的化学方程式为。
③E中盛有溶液。
(2)某同学将足量的SO2通入一支装有氧化钡溶液的试管,未见沉淀生成,若向该试管中加入加量(填字母),则可以看到白色沉淀产生。
| A.氨水 | B.稀盐酸 | C.稀硝酸 | D.氯化钙 |
(3)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4∶3;当Cl2的与含X的溶液完全反应后,有浅黄色沉淀产生,取上层清液加入氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式。
某同学想通过比较两种最高价氧化物对应水化物的酸性强弱来验证硫与碳的非金属性的强弱,他采用了如图所示的装置。请回答: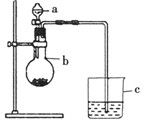
(1)仪器a的名称是,应盛放下列药品中的。
A.稀硫酸 B.亚硫酸
C.氢硫酸 D.盐酸
(2)仪器b的名称是,应盛放下列药品中的。
A.碳酸钙 B.硫酸钠
C.氯化钠 D.碳酸钠
(3)如果观察到C中的现象为,即可证明硫与碳的非金属性的强弱。