(1)已知X、Y、Z为第三周期元素,其原子的第一至第四电离能如下表:
| 电离能/kJ·mol-1 |
I1 |
I2 |
I3 |
I4 |
| X |
578 |
1 817 |
2 745 |
11 578 |
| Y |
738 |
1 451 |
7 733 |
10 540 |
| Z |
496 |
4 562 |
6 912 |
9 543 |
则X、Y、Z的电负性从大到小的顺序为 (用元素符号表示),元素Y的第一电离能大于X的第一电离能的原因是
。
(2)A、B、C、D是周期表中前10号元素,它们的原子半径依次减小。D能分别与A、B、C形成电子总数相等的分子M、N、W,且在M、N、W分子中,A、B、C三原子都采取sp3杂化。
①A、B、C的第一电离能由小到大的顺序为 (用元素符号表示)。
②M是含有 键的 分子(填“极性”或“非极性”)。
③N是一种易液化的气体,请简述其易液化的原因:
。
④W分子的VSEPR模型的空间构型为 ,W分子的空间构型为 。
⑤AB-中和B2分子的π键数目比为 。
(3)E、F、G三元素的原子序数依次增大,三原子的核外的最外层电子排布均为4s1。
①E元素组成的单质的晶体堆积模型为 (填字母)。
a.简单立方堆积 b.体心立方堆积
c.六方最密堆积 d.面心立方最密堆积
②F元素在其化合物中最高化合价为 。
③G2+的核外电子排布式为 ,G2+和N分子形成的配离子的结构式为 。
随着现代化工业的发展,能源问题已经越来越引起人们的重视。科学家预言,未来最理想的燃料是绿色植物,即将植物的秸秆(主要成分是纤维素)用适宜的催化剂作用水解成葡萄糖,再将葡萄糖转化为乙醇,用作燃料。
(1)写出绿色植物秸秆转化为乙醇的化学方程式:
①________________________________________________________________________;
②________________________________________________________________________。
(2)乙醇除用作燃料外,还可用来合成其他有机物,下列主要是以乙醇为起始原料的转化关系图。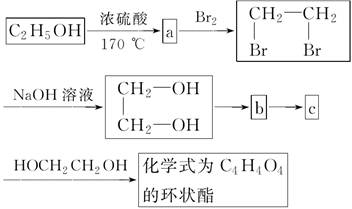
请写出上述物质的结构简式
a:______________、b:______________、c:______________。
(3)写出上面关系图中由c生成C4H4O4的化学方程式。(有机物用结构简式表示)
参考下列①~③回答问题。①皂化值是使1 g油脂皂化所需要的氢氧化钾的毫克数。
②碘值是使100 g油脂加成时消耗单质碘的克数。
③各种油脂的皂化值,碘值列表如下:
| 花生油 |
亚麻仁油 |
牛油 |
黄油 |
硬化大豆油 |
大豆油 |
|
| 皂化值 |
190 |
180 |
192 |
226 |
193 |
193 |
| 碘值 |
90 |
182 |
38 |
38 |
5 |
126 |
(1)单纯油(C17H33COO)3C3H5(相对分子质量884)形成的油,用氢氧化钾皂化时,皂化值为________,写出其反应方程式:________________________________。
(2)在下列①~③的括号内填入适当的词句。
①亚麻仁油比花生油所含的________脂肪酸多;(填写“饱和”或“不饱和”)
②黄油比牛油所含的________脂肪酸多;(填写“低级”或“高级”)
③硬化大豆油的碘值小的原因是________________________________;
④不同油脂的皂化值越大,则油脂的平均相对分子质量________;碘化值越高,则表明含________越多。
(3)为使碘值为180的100 g鱼油硬化,所需的氢气的体积在标准状况下为多少升?
(4)用下列结构简式所代表的酯,若皂化值为430,求n为多少?并完成下面反应方程式:
氮、磷、钾是植物生长的重要营养元素。洗衣粉中如加入多磷酸的钠盐作配料,虽能在洗衣时起软化水的作用,但使用此类洗衣粉会造成水质污染。
(1)硬水软化是指_______________________________________________________。
(2)若用肥皂洗衣,水的硬度不能太大,其原因是____________________。
(3)磷酸、焦磷酸、连三磷酸的结构简式依次是: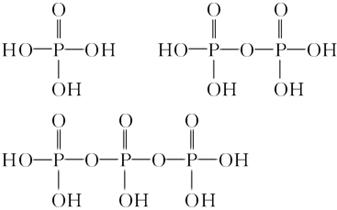
连多磷酸的通式为________(磷原子数用m表示)。
(4)含磷洗衣粉等生活污水排入河流造成水质污染的主要原因是______________________。
已知2 mol油酸、1 mol硬脂酸跟1 mol丙三醇完全反应,只生成一种甘油酯A,A的分子式为________,A可能的结构有________种。硬化1 mol A需标准状况下H2________ L,反应的化学方程式为________________________________________________________
_____________________________。
A在NaOH溶液中加热能发生________反应,反应的化学方程式为________________。
磷脂含有一个非极性基团和一个极性基团,水溶性的磷脂有重要的生物学功能。磷脂是甘油酯的一个 被
被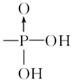 代替后,再与碱反应生成的产物。试将软脂酸和甘油转化成含Na+的磷脂。
代替后,再与碱反应生成的产物。试将软脂酸和甘油转化成含Na+的磷脂。
(1)________、(2)________、(3)________。