磷酸铁锂(LiFePO4)被认为是最有前途的锂离子电池正极材料。某企业利用富铁浸出液生成磷酸铁锂,开辟了处理硫酸亚铁废液一条新途径。其主要流程如下: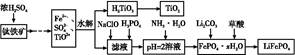
已知:H2TiO3是种难溶于水的物质。
(1)钛铁矿用浓硫酸处理之前,需要粉碎,其目的是 。
(2)TiO2+水解生成H2TiO3的离子方程式为 。
(3)加入NaClO发生反应的离子方程式为 。
(4)在实验中,从溶液中过滤出H2TiO3后,所得滤液浑浊,应如何操作 。
(5)为测定钛铁矿中铁的含量,某同学取经浓硫酸等处理的溶液(此时钛铁矿中的铁已全部转化为二价铁离子),采取KMnO4标准液滴定Fe2+的方法:(不考虑KMnO4与其他物质反应)在滴定过程中,若未用标准液润洗滴定管,则使测定结果 (填“偏高”、“偏低”或“无影响”),滴定终点的现象是 。滴定分析时,称取a g钛铁矿,处理后,用c mol/L KMnO4标准液滴定,消耗V mL,则铁元素的质量分数的表达式为 。
已知86Rn(氡)基态原子的电子排布式为1s22s22p63s23p63d104s24p64d104f145s25p65d106s26p6,88Ra基态原子的电子排布式可简化为[Rn]7s2。114号元素是化学家和物理学家很感兴趣的尚未发现的元素。
(1)用简化的形式写出114号元素基态原子的电子排布式: ______________
________________________________________________________________。
(2)根据原子核外电子排布的特征,判断114号元素在周期表中的第________周期________族。
(3)根据114号元素在周期表中的位置判断,它最不应具有的性质是________。
第一电离能大于88Ra
②鲍林电负性大于3.0
③最高化合价为+4价,也可有+2价
④最高价氧化物的对应水化物显碱性
下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。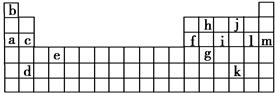
(1)下列________(填写编号)组元素的单质可能都是电的良导体。
①a、c、h②b、g、k③c、h、l④d、e、f
(2)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。
核外电子离开该原子或离子所需要的能量主要受两大因素的影响:
A.原子核对核外电子的吸引力
B.形成稳定结构的倾向
下表是一些气态原子失去核外不同电子所需的能量(kJ·mol-1):
| 锂 |
X |
Y |
|
| 失去第一个电子 |
519 |
502 |
580 |
| 失去第二个电子 |
7 296 |
4 570 |
1 820 |
| 失去第三个电子 |
11 799 |
6 920 |
2 750 |
| 失去第四个电子 |
—— |
9 550 |
11 600 |
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量__________________________________。
②表中X可能为以上13种元素中的(填写字母)____________元素。用元素符号表示X和j形成化合物的化学式________________。
③Y是元素周期表中第________族元素。
④以上13种元素中,________(填写字母)元素原子失去核外第一个电子需
要的能量最多。
根据下列五种元素的电离能数据(单位:kJ·mol-1),回答下面问题。
| 元素代号 |
I1 |
I2 |
I3 |
I4 |
| Q |
2 080 |
4 000 |
6 100 |
9 400 |
| R |
500 |
4 600 |
6 900 |
9 500 |
| S |
740 |
1 500 |
7 700 |
10 500 |
| T |
580 |
1 800 |
2 700 |
11 600 |
| U |
420 |
3 100 |
4 400 |
5 900 |
(1)在周期表中,最可能处于同一族的是()。
A.Q和R
B.S和T
C.T和U
D.R和T
E.R和U
(2)电解它们的熔融氯化物,阴极电极反应式最可能正确的是()。
A.Q2++2e-→Q
B.R2++2e-→R
C.S3++3e-→S
D.T3++3e-→T
E.U2++2e-→U
(3)它们的氯化物的化学式,最可能正确的是()。
A.QCl2
B.RCl
C.SCl3
D.TCl
E.UCl4
(4)下列元素中,化学性质和物理性质最像Q元素的是()。
A.硼(1s22s22p1)
B.铍(1s22s2)
C.锂1s22s1
D.氢(1s1)
E.氦(1s2)
有A、B、C、D四种短周期主族元素,它们的原子序数依次增大,其中A元素原子核外电子仅有一种原子轨道,也是宇宙中最丰富的元素,B元素原子核外p电子数比s电子数少1,C为金属元素且原子核外p电子数和s电子数相等,D元素的原子核外所有p轨道全充满或半充满。
(1)写出四种元素的元素符号:
A________,B________,C________,D________。
(2)写出C、D两种元素基态原子核外电子轨道表示式。
C_______________________________________________________________,
D_______________________________________________________________。
(3)写出B、C两种元素单质在一定条件下反应的化学方程式____________________________________________。
(4)写出B元素单质和氢化物的电子式:单质________,氢化物__________。
(1)19世纪末,人们开始揭示原子内部的秘密,最早发现电子的科学家是________。
(2)道尔顿的原子学说曾起了很大的作用。他的学说包含下列三个论点:①原子是不能再分的粒子,②同种元素的原子的各种性质和质量都相同,③原子是微小的实心球体。从现代的观点看,你认为三个论点中不确切的是________。