某研究性活动小组在实验室用三份不同初始浓度的氨基甲酸铵(NH2COONH4)溶液在不同温度下进行水解实验:NH2COONH4+2H2O NH4HCO3+NH3·H2O,经测得c(NH2COO-)与反应时间的关系如图所示。据图判断下列说法正确的是( )
NH4HCO3+NH3·H2O,经测得c(NH2COO-)与反应时间的关系如图所示。据图判断下列说法正确的是( )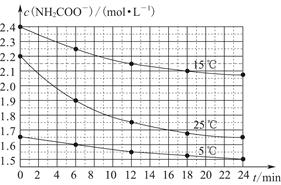
| A.0~12 min,初始浓度越大的实验,水解反应速率越大 |
| B.c(NH2COO-)将随反应时间的不断延长而一直减小至0 |
| C.25 ℃时0~6 min,v(NH2COO-)为0. 05 mol·L-1·min-1 |
| D.15 ℃时,第30 min时,c(NH2COO-)为2.0 mol·L-1 |
下表中元素均为中学化学常见短周期元素根据表中信息,下列说法不正确的是
| 元素代号 |
X |
Y |
Z |
W |
N |
| 原子半径/nm |
0.186 |
0.074 |
0.102 |
0.099 |
0.16 |
| 主要化合价 |
+1 |
-2 |
-2+6 |
+7-1 |
+2 |
A.X和W形成的化合物是共价化合物
B.常温下单质与水反应速率X大于N
C.最高价氧化物对应水化物酸性W大于Z
D.X和Y的单质在一定条件下反应可生成一种淡黄色的固体化合物
同周期相邻主族的两种元素的核外电子数不可能相差
| A.1 | B.8 | C.11 | D.25 |
某元素X的逐级电离能如下图所示,下列说法正确的是
| A.X元素可能为+4价 |
| B.X为非金属 |
| C.X为第五周期元素 |
| D.X与氯反应时最可能生成的阳离子为X3+ |
核磁共振(NMR)技术已广泛应用于复杂分子结构测定和医学诊断等高科技领域。已知只有质子数和中子数均为奇数的原子核有NMR现象。试判断下列原子均可产生NMR现象的是
| A.18O31P119Sn |
| B.27Al19F12C |
| C.80Br2H14N |
| D.元素周期表中第一周期所有元素的原子 |
某主族元素的原子最外层电子排布是5S1,下列描述中正确的是
| A.其单质常温下跟水反应不如钠剧烈 |
| B.其原子半径比钾原子半径小 |
| C.其碳酸盐易溶于水 |
| D.其氢氧化物不能使氢氧化铝溶解 |