人体血液里Ca2+离子的浓度一般采用mg/mL来表示。加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定,使草酸转化成CO2逸出。
试回答:
(1)现需要80 mL 0.02 mol·L-1标准KMnO4溶液来进行滴定,则配制溶液时需要的玻璃仪器有烧杯、玻璃棒和______________________;配制时, KMnO4溶液应用强酸酸化,本实验选择________作酸化剂。若选择HNO3酸化,则结果可能________(填“偏大”“偏小”或“不变”)。
(2)草酸与KMnO4反应的离子方程式为______________________________________
(3)滴定时,根据现象___________________________________
即可确定反应达到终点。
(4)滴定的实验数据如下所示:
| 实验编号 |
待测血液的体积/mL |
滴入KMnO4溶液的体积/mL |
| 1 |
20.00 |
11.95 |
| 2 |
20.00 |
13.00 |
| 3 |
20.00 |
12.05 |
经过计算,血液样品中Ca2+离子的浓度为________mg/mL。
(5)滴定的方法有酸碱中和滴定、沉淀滴定、络合滴定等。沉淀滴定所用的指示剂本身就是一种沉淀剂。以AgNO3标准溶液测定Cl-为例:
终点前:Ag++Cl-=AgCl (白色)
终点时:2Ag++CrO42—=Ag2CrO4(砖红色)
这是因为AgCl溶解度比Ag2CrO4更________的缘故。
乙酰苯胺可用作止痛剂、退热剂、防腐剂和染料中间体,实验室制备乙酰苯胺反应原理和有关数据如下: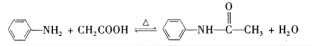
| 名称 |
相对分子质量 |
性状 |
密度(g/cm3) |
沸点/℃ |
溶解度 |
|
| 苯胺 |
93 |
无色油状液体具有还原性 |
1.02 |
184 |
微溶于水 |
均易溶于乙醇、乙醚 |
| 乙酸 |
60 |
无色液体 |
1.05 |
118 |
易溶于水 |
|
| 乙酰苯胺 |
135 |
白色晶体 |
1.22 |
304 |
微溶于冷水、溶于热水 |
实验步骤:
在50ml圆底烧瓶中加入无水苯胺5ml.,冰醋酸7.5mL,锌粉0.lg,按下图安装仪器,加入沸石,给反应器均匀加热,使反应液在微沸状态下回流,调节加热温度,使柱顶温度控制在105℃左右,反应约60~ 80nun,当反应基本完成时,停止加热.
在搅拌下,趁热将烧瓶中的物料倒人盛有l00mL冰水的烧杯中,剧烈搅拌,并冷却烧杯至室温,粗乙酰苯胺结晶析出,抽滤、洗涤、干燥,得到乙酰苯胺粗品.将粗品重结晶,抽滤,晾干,称重,计算产率,注:D为刺形分馏柱,用于沸点差别不太大的混合物的分离.
请回答下列问题:
(1)仪器B的名称。
(2)装置图中加热可用(填“水浴”或“油浴”)。
(3)实验中加入锌粉的目的是。
(4)为何要控制分馏柱上端的温度在105℃左右。
(5)通过观察到,现象可判断反应基本完成,反应结束后须立即倒入事先准备好的冰水中的原因。
(6)洗涤乙酰苯胺粗品最合适的试剂是。
a.用少量冷水洗
b.用少量热水洗
c.先用冷水洗,再用热水洗
d.用酒精洗
(7)该实验最终得到纯品1.8 g,则乙酰苯胺的产率是。
草酸(H2C2O4)是一种白色固体,熔点是101℃~102℃,大约在157℃时开始升华,189.5℃分解,是常用的工业原料。利用草酸和含镍废料(镍铁钙镁合金为主)制取草酸镍。已知草酸的钙、镁、镍盐难溶于水。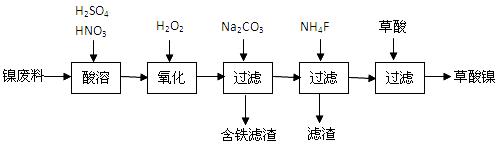
(1)生产过程中多次进行过滤。实验室进行过滤操作中用到铁架台、烧杯、玻璃棒,还需要;
(2)加入过氧化氢后缓慢加入碳酸钠溶液调pH至4.0 ~ 4.5左右,加入碳酸钠溶液的作用是,
再加入NH4F的目的是;
(3)用下图所示仪器连接组成的装置来探究草酸受热分解的产物。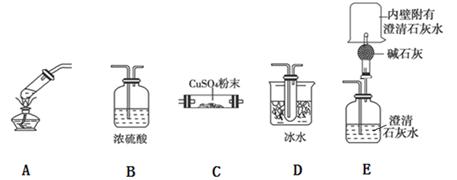
①实验中,观察到无水硫酸铜变蓝,洗气瓶中内澄清石灰水变浑浊,在干燥管尖嘴处点燃逸出的气体,烧杯内壁附有的澄清石灰水变浑浊,证明产物中有______________;E装置略作改动也能证明产物中无氢气,证明方法是______________________________;
②装置的连接顺序为__________________,C装置的作用是____________________。
(13分)重铬酸钾是一种重要的氧化剂,工业上常用铬铁矿(主要成分为FeO·Cr2O3、SiO2、Al2O3)为原料生产。实验室模拟工业法用铬铁矿制重铬酸钾(K2Cr2O7)的主要工艺如下: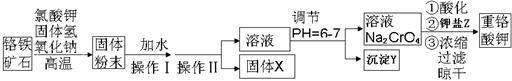
试回答下列问题:
(1)以上工艺流程所涉及元素中属于过渡元素的有。铁在周期表的位置是。
(2)操作Ⅱ的名称是。
(3)固体X的主要成分是___________,沉淀Y的主要成分是。
(4)流程中①酸化所用的酸和②钾盐Z最合适的是(填符号)________,
| A.盐酸和氯化钾 | B.硫酸和氯化钾 |
| C.硫酸和硫酸钾 | D.次氯酸和次氯酸钾 |
酸化反应的离子方程式为。
(5)FeO·Cr2O3与氯酸钾、氢氧化钠高温反应化学方程式:。
(14分)肼是重要的化工原料。某探究小组利用下列反应制取水合肼(N2H4·H2O)。
CO(NH2)+2NaOH+NaClO = Na2CO3+N2H4·H2O+NaCl
实验一:制备NaClO溶液
(1)将氯气通入到盛有NaOH的锥形瓶中,锥形瓶中发生反应的离子方程式是;
实验二:制取水合肼(实验装置如图所示)
控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应。加热蒸馏三颈烧瓶内的溶液,收集108~114 ℃馏分。(已知:N2H4·H2O+2NaClO = N2↑+3H2O+2NaCl)
(2)分液漏斗中的溶液是(填标号A或B);
A.NaOH和NaClO混合溶液
B.CO (NH2) 2溶液
选择的理由是;
实验三:测定馏分中肼含量
水合肼具有还原性,可以生成氮气。测定水合肼的质量分数可采用下列步骤:
a.称取馏分5.000 g,加入适量NaHCO3固体,经稀释、转移、定容等步骤,配制250 mL溶液。
b.移取25. 00 mL于锥形瓶中,加入10 mL水,摇匀.
c.用0.2000 mol/L碘溶液滴定至溶液出现微黄色且半分钟内不消失,滴定过程中,溶液的pH保持在6.5左右。记录消耗碘的标准液的体积。
d.进一步操作与数据处理
(3)水合肼与碘溶液反应的化学方程式;滴定过程中,NaHCO3能控制溶液的pH在6.5左右,原因是;
(4)滴定时,碘的标准溶液盛放在 滴定管中(选填:“酸式”或“碱式”) ;若本次滴定消耗碘的标准溶液为18.00 mL,馏分中水合肼(N2H4·H2O)的质量分数为(保留三位有效数字);
(5)为获得更可靠的滴定结果,步骤d中进一步操作主要是:。
(1)某研究性学习小组用一定物质的量浓度的盐酸滴定10.00 mL一定物质的量浓度的NaOH溶液,滴定时使用pH计精确测量滴定过程中溶液的pH变化(温度为25℃),并绘制出滴定过程中溶液pH的变化曲线如下图所示。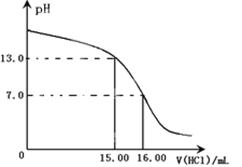
实验过程中需要使用的仪器有铁架台、滴定管夹、、、________、,由图可计算出标准HCl溶液的物质的量浓度为___________(忽略溶液混合时的体积变化)。
(2)该小组同学在探究上述NaOH溶液与酚酞溶液作用时,发现了一个意外现象:向少量酚酞溶液中滴加NaOH溶液,开始时溶液变红色,但继续滴加NaOH溶液至一定量时红色消失。对此意外现象形成的原因,该小组同学分别提出了各自的看法并进行相应的实验设计。
甲:可能是NaOH溶液与空气中的CO2反应造成的。
乙:可能是溶液在碱性条件下继续与空气中的氧气反应造成的。
丙:可能与NaOH溶液的浓度有关。
【理论分析】①乙同学认为甲同学的猜想明显错误,他的理由是__________ _____。
【实验设计】②为证实乙同学的猜想,还需做如下实验,请完成下表:
| 实验步骤 |
设计此步骤的目的 |
| 将配制的NaOH溶液加热 |
|
| 在加热后的溶液中滴加酚酞,并在上方滴加一些植物油 |
③通过以上实验,三位同学看到:溶液先变成红色,一会儿红色消失。因此溶液褪色与氧气无关。若丙同学的猜想正确,请你设计一个简单的实验加以证明(按要求填写在下表中):
| 实验方案 |
观察到的现象和结论 |