碳铵是一种较常使用的化肥,它在常温下易分解。某化学兴趣小组对碳铵的成分存在疑问,进行了如下探究。
【定性实验】检验溶液中的阴、阳离子。
取少量固体放入试管中,加入盐酸,把生成的气体通入澄清石灰水中,有白色沉淀生成。再另取少量碳铵放入试管中,加入浓NaOH溶液,加热,用湿润的红色石蕊试纸检验生成的气体,石蕊试纸变蓝色。
(1)根据实验现象,推测碳铵中所含有阴离子可能是 和 。
(2)据实验现象,碳铵与足量NaOH溶液加热反应的离子方程式可能是 。
【定量实验】测定碳铵中C元素和N元素质量比。
该兴趣小组准确称取ag碳铵,加热使之分解,并把产物通入碱石灰中,如下图所示。
(1)碳铵固体应放在 中进行加热。
| A.试管 | B.蒸发皿 | C.烧瓶 | D.坩埚 |
(2)从安全的角度考虑,尾气处理的装置可以选用 。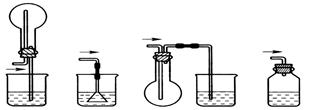
A B C D
(3)若灼烧后没有固体残余,称量U形管在实验前后的质量差为bg。由此测得N元素的质量是 g。
(4)为了测定碳铵中碳元素的质量,他们设计的实验方案是将ag碳铵完全溶解于水,加入过量BaCl2,然后测定生成沉淀质量。请你评价该方案是否合理。 (填“合理”“不合理”),理由是 。
相关物质性质如下表所示:
| 物质 |
熔点/℃ |
沸点/℃ |
相对密度(20℃) |
毒性 |
水溶性 |
| 苯 |
5.5 |
80.1 |
0.8794 |
有 |
不溶于水 |
| 硝酸 |
-41.59 |
83 |
1.503 |
易溶于水 |
|
| 硝基苯 |
5.7 |
210.9 |
1.205 |
有 |
不溶于水 |
可供选择的实验用品:
①仪器:烧杯、大试管、铁架台(带铁圈)、石棉网、酒精灯、橡皮塞、玻璃管、温度计、分液漏斗等。
②药品:浓硝酸、稀硝酸、浓硫酸、稀硫酸、苯、5%NaOH溶液、蒸馏水等。
请参考以下实验设计思路,讨论并回答有关问题。
(2)选择合适的实验仪器及条件
①采用的加热方式:
________________________________________________________________________,
其优点是
________________________________________________________________________。
②反应物均为________,采用________作反应器。
③反应过程中由于有易挥发的物质,为防止损失采用________,其兼起________作用。
④用________来控制________的温度。
⑤请画出实验装置简图。
(2)安排合理的实验步骤
①按装置图组装好实验仪器。
②在大试管里,先加入1.5 mL浓硝酸和2 mL浓硫酸,摇匀,冷却到50~60℃。
③再慢慢滴入1 mL苯,不断轻轻摇动,使之混合均匀,塞好单孔塞。
④放在50~60℃的水浴中加热10 min。
(3)产品提纯
探究讨论:①浓硝酸和浓硫酸的混合顺序能否颠倒?为什么?
________________________________________________________________________。
②浓硫酸的作用是
________________________________________________________________________。
(11分)(2011·滨州模拟)Ⅰ.回答下列有关常数的问题:
(1)Kw的数学表达式是________,温度升高Kw________(选填“变大”“变小”或“不变”),若定义pOH=-lgc(OH-),则pH+pOH=________(用含Kw的代数式表示)。
(2)Ka通常表示弱酸的电离平衡常数,Ka值越大表示该弱酸的酸性________。α通常称为电离度,顾名思义是表示弱电解质的电离程度大小的一个指标,对于某一元弱酸,当用蒸馏水稀释该酸时,Ka________(选填“变大”“变小”或“不变”)。α________(选填“变大”“变小”或“不变”)。
(3)Ksp表示难溶物的溶度积常数,该常数越大表示________。
Ⅱ.已知常温下,AgBr的Ksp=4.9×10-13mol2·L-2、AgI的Ksp=8.3×10-17mol2·L-2。
(1)现向含有AgI的饱和溶液中:
①加入固体AgNO3,则c(I-)________(填“变大”“变小”或“不变”,下同);
②若改加更多的AgI,则c(Ag+)________;
③若改加AgBr固体,则c(I-)______;而c(Ag+)______。
(2)有关难溶盐的溶度积及溶解度(与AgBr、AgI无关),有以下叙述,其中正确的是________。
| A.两种难溶盐电解质,其中Ksp小的溶解度一定小 |
| B.向含有AgCl固体的溶液中加入适量的水使AgCl溶解又达到平衡时,AgCl的溶度积不变,其溶解度也不变 |
| C.将难溶电解质放入纯水中,溶解达到平衡时,电解质离子的浓度的乘积就是该物质的溶度积 |
| D.溶液中存在两种可以与同一沉淀剂生成沉淀的离子,则Ksp小的一定先生成沉淀 |
E.难溶盐电解质的Ksp与温度有关
F.同离子效应(加入与原电解质具有相同离子的物质),使难溶盐电解质的溶解度变小,也使Ksp变小
(3)现向含有NaBr、KI均为0.002 mol·L-1的溶液中加入等体积的浓度为4×10-3 mol/L AgNO3溶液,则产生的沉淀是________(填化学式);若向其中再加入适量的NaI固体,则最终可发生沉淀转化的总反应方程式表示为:______________________________。
(8分)常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
| 实验 编号 |
HA物质的量 浓度(mol· L-1) |
NaOH物质的 量浓度(mol· L-1) |
混合溶液的 pH |
| 甲 |
0.2 |
0.2 |
pH=a |
| 乙 |
c1 |
0.2 |
pH=7 |
| 丙 |
0.2 |
0.1 |
pH>7 |
| 丁 |
0.1 |
0.1 |
pH=9 |
请回答:
(1)不考虑其他组的实验结果,单从甲组情况分析,
若a________7(填“>”、“<”或“=”),则HA为强酸;
若a________7(填“>”、“<”或“=”),则HA为弱酸。
(2)在乙组中混合溶液中离子浓度c(A-)与c(Na+)的大小关系是( )
| A.前者大 | B.后者大 |
| C.二者相等 | D.无法判断 |
(3)从丙组实验结果分析,HA是________酸(填“强”或“弱”)。该混合溶液中离子浓度由大到小的顺序是___________________________________________。
(4)丁组实验所得混合溶液中由水电离出的c(OH-)=________mol·L-1。
(8分)Ⅰ.(1)饱和氯化铵溶液显酸性,原因是
________________________________________________________________________
________________________________________________________________________;
向饱和氯化铵溶液中加入少量Mg(OH)2固体,固体完全溶解;其合理的解释(用相关离子方程式表示)为
________________________________________________________________________
________________________________________________________________________。
(2)向Mg(OH)2悬浊液中加入适量CH3COONH4溶液,
Mg(OH)2能否完全溶解________(填“能”或“否”),理由是
________________________________________________________________________
________________________________________________________________________。
Ⅱ.硫酸是强酸,中学阶段将硫酸在水溶液中看作完全电离。但事实是,硫酸在水中的第一步电离是完全的,第二步电离并不完全,其电离情况为:H2SO4===H++HSO4-,HSO4-===H++SO42-。
请回答下列有关问题:
(1)Na2SO4溶液呈________(填“弱酸性”“中性”或“弱碱性”),其理由是________________________________________________________________________
(用离子方程式表示);
(2)H2SO4溶液与BaCl2溶液反应的离子方程式为
________________________________________________________________________
________________________________________________________________________。
(3)在0.10 mol·L-1的Na2SO4溶液中,下列离子浓度关系正确的是________(填写编号);
| A.c(Na+)=c(SO42-)+c(HSO4-)+c(H2SO4) |
| B.c(OH-)=c(HSO4-)+c(H+) |
| C.c(Na+)+c(H+)=c(OH-)+c(HSO4-)+2c(SO42-) |
| D.c(Na+)=2c(SO42-)+2c(HSO4-) |
(4)写出NaHSO4溶液中溶质电离常数(Ka)的表达式________________;
(5)若25℃时,0.10 mol·L-1的NaHSO4溶液中c(SO2-4)=0.029 mol·L-1,则0.10 mol·L-1的H2SO4溶液中c(SO42-)________0.029 mol·L-1(填“<”“>”或“=”),其理由是________________________________________________________________________;
(6)如果25℃时,0.10 mol·L-1H2SO4溶液的pH=
-lg 0.11,则0.10 mol·L-1的H2SO4溶液中c(SO42-)=________mol·L-1。
(8分)用中和滴定法测定某烧碱样品的纯度,试根据实验回答下列问题:
(1)准确称量8.2 g含有少量中性易溶杂质的样品,配成500 mL待测溶液。称量时,样品可放在________(填编号字母)称量。
A.小烧杯中 B.洁净纸片上 C.托盘上
(2)滴定时,用0.2000 mol·L-1的盐酸来滴定待测溶液,不可选用________(填编号字母)作指示剂。
A.甲基橙 B.石蕊
C.酚酞 D.甲基红
(3)滴定过程中,眼睛应注视______________;在铁架台上垫一张白纸,其目的是________________________________________________________________________
________________________________________________________________________。
(4)根据下表数据,计算被测烧碱溶液的物质的量浓度是________mol·L-1,烧碱样品的纯度是________。
| 滴定次数 |
待测溶液 体积(mL) |
标准酸体积 |
|
| 滴定前的刻度 (mL) |
滴定后的刻度 (mL) |
||
| 第一次 |
10.00 |
0.40 |
20.50 |
| 第二次 |
10.00 |
4.10 |
24.00 |
(5)下列实验操作会对滴定结果产生什么影响(填“偏高”、“偏低”或“无影响”)?
①观察酸式滴定管液面时,开始俯视,滴定终点平视,则滴定结果________。
②若将锥形瓶用待测液润洗,然后再加入10.00 mL待测液,则滴定结果________。