A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
| 阳离子 |
Na+、K+、Cu2+ |
| 阴离子 |
S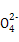 、OH- 、OH- |
如图1所示装置中,甲、乙、丙三个烧杯中依次盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加了16 g。常温下各烧杯中溶液的pH与电解时间t的关系如图2所示。请回答下列问题: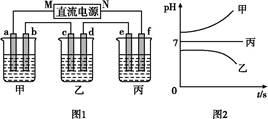
(1) M为直流电源的 极,b电极上发生的电极反应为 。
(2)计算e电极上生成的气体在标准状况下的体积为 。
(3)写出乙烧杯中的总反应的离子方程式: 。
(4)要使丙烧杯中的C溶液恢复到原来的状态,需要进行的操作是(写出要加入的物质和质量) 。
现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg·mol-1。若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为________mol。
(2)该气体所含原子总数为________个。
(3)该气体在标准状况下的体积为____________L。
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为_______。
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为_____mol·l-1。
选择下列实验方法分离物质,将分离方法的序号填在横线上
A 萃取分液法 B 结晶法 C 分液法 D 蒸馏法 E 过滤法
①_____分离饱和食盐水与沙子的混合物。
②_____分离水和汽油的混合物。
③_____分离四氯化碳(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物。
④____从碘的水溶液里提取碘。
⑤_____从硝酸钾和氯化钠的混合液中获得硝酸钾。
通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下: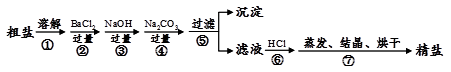
(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是。
(2)第②步操作的目的是除去粗盐中的(填化学式,下同),第⑥步操作的目的是除去滤液中。
(3)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、、(填化学式)。
(4)判断加入的盐酸“适量”的方法是。
(5)第③步的化学方程式为__________________________________________
第④步的化学方程式为______________________________、_______________________________
用18mol/L 浓硫酸配制240 ml 3.0mol/L 稀硫酸的实验步骤如下:
① 计算所用浓硫酸的体积 ② 量取一定体积的浓硫酸
③ 稀释 ④ 转移 ⑤ 洗涤⑥定容⑦摇匀
请回答下列问题
(1)所需浓硫酸的体积是,配置溶液的容量瓶的规格是
(从下列中选用A.100ml B.250ml C.500ml D.1000ml)
(2)使用容量瓶前必须进行的一步操作是_____________________
(3)第③步实验的操作是
(4)第⑥步实验的操作是
(5)下列情况对所配制的稀硫酸浓度有何影响?(用偏大、偏小、无影响填写)
A.所用的浓硫酸长时间放置在密封不好的容器中
B.容量瓶用蒸馏洗涤后残留有少量的水
C.所用过的烧杯、玻璃棒未洗涤
D.定容时俯视溶液的液凹面
同温同压下,等质量的SO2和O2,两者体积比为_________,分子个数比为________,密度比为__________。