某学习兴趣小组探究氨气的制取实验:
(1)甲同学拟用下列实验方法制备氨气,其中合理的是 (填序号,下同)。
| A.将氯化铵固体加热分解 |
| B.将浓氨水滴入氢氧化钠固体中 |
| C.将氢氧化钠固体加入浓氨水中 |
| D.将氯化铵稀溶液滴入氢氧化钠固体中 |
(2)如图是甲同学设计收集氨气的几种装置,其中可行的是 ,集气的原理是 。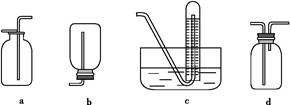
某校化学课外兴趣小组的学生为了验证乙醇的分子结构,设计如下实验程序:乙醇组成元素的测定、分子式的测定、分子结构的测定。
(1)他们决定用燃烧乙醇分析产物来确定乙醇中含有C、H两种元素。简要说明他们的具体操作:①证明含有氢元素的操作是_________________________________________________________
________________________________________________________________________________________;
②证明含有碳元素的操作是________________________________________________
_______________________________________________________________________
(2)要用燃烧分析产物证实乙醇中还含有氧元素时,需取得一些实验数据,这些数据应该是________________________。
(3)为确定乙醇的分子式,除(2)中数据外,还需不需要测定乙醇的相对分子质量?
_______________________________________________________________________
(4)为测定乙醇分子结构,他们用了无水乙醇和金属钠反应收集生成氢气的方法,选用了如下图所示的仪器(有的仪器配用双孔橡皮塞)。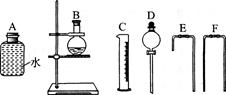
①装置的连接顺序是______接______接______接______接_______接_______。
②已知无水酒精的密度为0.789 g·cm一3,移取2.0mL酒精,反应完全后(钠过量),收集390 mL气体。则乙醇分子中能被钠取代出的氢原子数为_______,由此可确定乙醇的结构为______________________而不是______________。
(5)实验所测定的结果偏高,可能引起的原因是(填写编号)。______________
A.本实验在室温下进行
B.无水酒精中混有微量甲醇
C.无水酒精与钠反应不够完全
实验需要0.1 mol/L NaOH溶液450 mL,根据溶液配制中的情况回答下列问题:
(1)实验中除了托盘天平、烧杯、容量瓶外还需要的其他仪器有______
_________________________________________________________。
(2)根据计算得知,所需NaOH的质量为________g。
(3)配制一定物质的量浓度溶液的实验中,如果出现以下操作
| A.称量时用了生锈的砝码 |
| B.将NaOH放在纸张上称量 |
| C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中 |
| D.往容量瓶转移时,有少量液体溅出 |
E.未洗涤溶解NaOH的烧杯
F.定容时仰视刻度线
G.容量瓶未干燥即用来配制溶液
H.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
对配制的溶液物质的量浓度大小可能造成的影响是(填写字母)偏大的有________。
现有NaHCO3和Na2CO3·xH2O的混合物,为了测定x值,某同学采用如图所示的装置进行实验(CaCl2、碱石灰均足量)。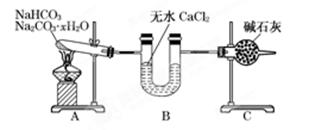
(1)A装置的作用:________________________________________________________________。
(2)B装置的作用是:_______________________________________________________________。
(3)C装置的作用是:_________________________________________________________________。
(4)若在装置A的试管中装入NaHCO3和Na2CO3·xH2O的混合物3.7 g,用酒精灯加热到反应完全,此时B管增重1.89g,C管增重0.22 g,则x的值为______。
(5)该装置还不是很完善,可能使测定结果偏小,应如何改进________。为什么?___________________________________________________________________________________。
下图是实验室制取并收集Cl2的装置。A是Cl2发生装置,,E是硬质玻璃管中装有铜丝网;F为干燥的广口瓶,烧杯G为尾气吸收装置。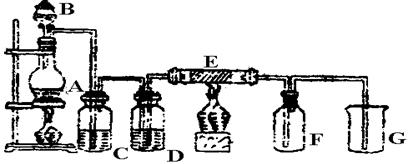
试回答:
(1)A中发生的化学反应的离子方程式为。
(2)C、G中各装的药品:C__________;G__________。
(3)E反应方程式为。
(4)写出G中反应的离子方程式。
(5)若将Cl2和SO2等物质的量混合漂白作用减弱,用化学方程式解释原因。
正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛。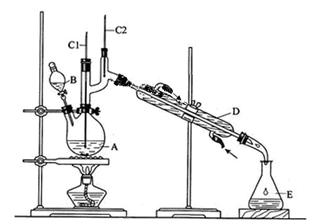
发生的反应如下:
反应物和产物的相关数据列表如下:
| 沸点/℃ |
密度/g·cm-3 |
水中溶解性 |
|
| 正丁醇 |
117.2 |
0.8109 |
微溶 |
| 正丁醛 |
75.7 |
0.8017 |
微溶 |
实验步骤如下:
将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中。在A中加入4.0g正丁醇和几粒沸石,加热。当有蒸汽出现时,开始滴加B中溶液。滴加过程中保持反应温度为90~95℃,在E中收集90℃以上的馏分。
将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77℃馏分,产量2.0g。回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,说明理由。
(2)加入沸石的作用是,若加热后发现未加入沸石,应采取的正确方法是。
(3)上述装置图中,B仪器的名称是,D仪器的名称是。
(4)将正丁醛粗产品置于分液漏斗中分水时,水在层(填“上”或“下”)。
(5)反应温度应保持在90~95℃,其原因是。
(6)本实验中,正丁醛的产率为%。