(1)如图1是一种新型燃料电池,它以CO为燃料,一定比例的Li2CO3和Na2CO3熔融混合物为电解质,图2是粗铜精炼的装置图,现用燃料电池为电源进行粗铜的精炼实验。
回答下列问题:
①写出A极发生的电极反应式______________________________________。
②要用燃料电池为电源进行粗铜的精炼实验,则B极应与________极相连(填“C”或“D”)。
③当消耗标准状况下2.24 L CO时,C电极的质量变化为________。
(2)工业上,可用铁作阳极,电解KOH溶液制备K2FeO4。
①电解过程中,OH-向________(填“阴”或“阳”)极移动,阳极的电极反应式为____________________________。
②若阳极有28 g Fe溶解,则阴极析出的气体在标准状况下的体积为________L。
烷基苯在高锰酸钾的作用下,侧链被氧化成羧基,例如: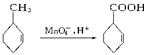 。化合物A—E的转化关系如图所示,已知:A是芳香化合物,只能生成3种一溴代物,B有酸性,C是常用增塑剂,D是有机合成的重要中间体和常用化学试剂(D也可由其他原料催化氧化得到)。
。化合物A—E的转化关系如图所示,已知:A是芳香化合物,只能生成3种一溴代物,B有酸性,C是常用增塑剂,D是有机合成的重要中间体和常用化学试剂(D也可由其他原料催化氧化得到)。
写出A、B、C、D的结构简式:___________、___________、___________、___________。
卤代烃在氢氧化钠存在的条件下水解,这是一个典型的取代反应,其实质是带负电的原子团(例如OH-等阴离子)取代卤代烃中的卤原子。例如:
CH3CH2CH2Br+OH-(或NaOH) CH3CH2CH2—OH+Br-(或NaBr)
CH3CH2CH2—OH+Br-(或NaBr)
写出下列反应的化学方程式:
(1)溴乙烷跟NaHS反应______________________________________________________。
(2)碘甲烷跟CH3COONa反应_________________________________________________。
(3)由碘甲烷、无水乙醇和金属钠合成甲乙醚(CH3—O—CH2CH3)。_______________。
某芳香族化合物A的分子式为C7H6O2,溶于NaHCO3水溶液,将此溶液加热,能用石蕊试纸检验出有酸性气体产生。
(1)由此推断出A的结构简式为________________________________________________。
(2)写出有关反应的化学方程式:_______________________________________________。
(3)A有_________个属于芳香族化合物的同分异构体,它们的结构简式为____________。
(1)今有A、B、C三种二甲苯;将它们分别进行一硝化反应,得到的产物分子式都是C8H9NO2,但A得到两种产物,B得到三种产物,C只得到一种产物。由此可以判断A、B、C各是下列哪一种结构,请将字母填入结构式后面的括号中。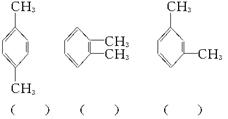
(2)请写出一个化合物的结构简式。它的分子式也是C8H9NO2,分子中有苯环,苯环上有三个取代基,其中之一为羧基,但并非上述二甲苯的硝化产物。请任写一个:______________________。
(1)短周期的元素A、B,A原子最外层电子为a个,次外层电子为b个;B原子M层电子为(a-b)个,L层为(a+b)个。则A为______________,B为______________。
(2)已知X元素L层比Y元素L层少3个电子,Y元素原子核外电子总数比X元素多5个,则X、Y分别为______________、______________。