大气中硫、氮的氧化物是形成酸雨的主要物质。某地酸雨中可能含有下列离子:Na+、Ba2+、NH4+、Al3+、Cl-、SO32-、SO42-、NO3-等。某研究小组取该地一定量的酸雨,浓缩后将所得澄清试液分成三份,进行如下实验:
| 试样 |
所加试剂 |
实验现象 |
| 第一份试液 |
滴加适量的淀粉KI溶液 |
溶液呈蓝色 |
| 第二份试液 |
滴加用盐酸酸化的BaCl2溶液 |
有白色沉淀产生 |
| 第三份试液 |
滴加NaOH溶液,加热,加入的NaOH溶液体积(V)与生成的沉淀、产生的气体的物质的量(n)的关系如右图 |
 |
请回答下列问题:
(1)根据实验结果判断该酸雨中肯定不存在的离子是______________,不能确定的离子有________________。
(2)写出第一份试液滴加淀粉KI溶液时发生反应的离子方程式:__________________。
(3)第三份试液滴加NaOH溶液,加热,整个过程中发生了多个反应,写出其中两个反应的离子方程式:__________________________________、__________________________。
(4)设计实验方案,检验该酸雨中是否存在Cl-:___________________________________
______________________________。
(5)该小组为了探究NO参与硫酸型酸雨的形成过程,在烧瓶中充入含有少量NO的SO2气体,再慢慢通入O2,发生化学反应后,再喷洒适量蒸馏水即得硫酸型酸雨,则NO在上述反应中的作用是________________________________________________________。
铁、铜单质及其化合物应用范围很广。现有含氯化亚铁杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按如图步骤进行提纯: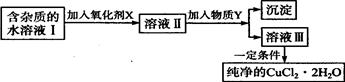
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH,见下表:
| Fe3+ |
Fe2+ |
Cu2+ |
|
| 氢氧化物开始沉淀时的pH |
1.9 |
7.0 |
4.7 |
| 氢氧化物完全沉淀时的pH |
3.2 |
9.0 |
6.7 |
请回答下列问题。
(1)加入氧化剂的目的是。
(2)最适合作氧化剂X的是。
A.K2Cr2O7B.NaClO C.H2O2D.KMnO4
(3)加入的物质Y是。
(4)若不用物质Y而是直接用碱能不能达到目的?(填“能”或“不能”)。若能,不用回答;若不能,试解释原因:。
(5)最后能不能直接蒸发结晶得到CuCl2·2H2O晶体?(填“能”或“不能”)。若能,不用回答;若不能,回答该如何操作? 。
(6)若向溶液Ⅱ中加入碳酸钙,产生的现象是。
(7)若向溶液Ⅱ中加入镁粉,产生的气体是。试解释原因:。
(8)FeCl3溶液具有净水作用的原因是。
有机物D是一种合成抗高血压药的重要通用中间体,其合成路线如下:(已知A是一种芳香酸)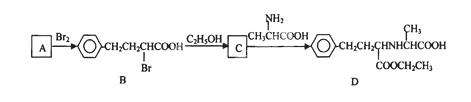
(1)A、C的结构简式分别是、。D中含有的含氧官能团名称是。
(2)C→D的反应类型是。
(3)加热条件下,C在足量NaOH水溶液中反应的化学方程式是。
(4)E是一种相对分子质量比A小14的芳香酸。写出满足下列条件的E的所有同分异构体的结构简式:。
①能发生银镜反应 ②一定条件下可发生水解反应 ③分子的核磁共振氢谱中有四组峰。
(5)F是B在碱溶液中水解后再酸化的产物。F在一定条件下可聚合成高分子化合物,写出该反应的化学方程式。
发展低碳经济,构建低碳社会。科学家们提出利用以工业废气中的CO2为原料,以CuO与ZnO混合物为催化剂,其反应为:CO2+3H2 CH3OH + H2O。
CH3OH + H2O。
(1)某温度下,在体积为l L的密闭容器中充入lmol CO2和4molH2,测得CO2和CH3OH(g)的浓度随时间变化如Ⅰ图所示。从反应开始到平衡,甲醇的平均反应速率v(CH3OH)=;氢气的转化率为。
(2)常温常压下已知下列反应的能量变化如Ⅱ图所示:写出由二氧化碳和氢气制备甲醇的热化学方程式:,该反应的△S___0(填“>”或“<”或“=”);反应达到平衡后,要使该平衡向右移动,其它条件不变时,可以采取的措施有(填序号)。
| A.缩小反应器体积 | B.升高温度 |
| C.恒容条件下通入CO2 | D.使用合适的催化剂 |
(3)在实际生产中发现,随着甲醇的生成,还伴随有少量CO等副产物出现,且CO2的转化率、甲醇和CO的含量还受气体混合物在反应锅炉内的流动速率、催化剂CuO的质量分数影响。通过实验分别得到如下图。
①由图Ⅲ得,生产甲醇的气体最佳流动速率为L•h-1;
②已知当催化剂中没有CuO,只有单组份ZnO时,反应速率最大。说明为什么不选择单组份ZnO的原因,根据图Ⅳ判断,催化剂CuO的质量分数最好为%。
(I)研究CO2的利用对促进低碳社会的构建具有重要的意义。将CO2与焦炭作用生成
CO,CO可用于炼铁等。
(1)已知:Fe2O3(s) + 3C(石墨) =2Fe(s) + 3CO(g) △H 1 =+489 kJ/mol
C(石墨)+CO2 (g)=2CO(g) △H 2 = +172 kJ/mol
则Fe2O3(s) + 3CO(g) = 2Fe (s) + 3CO2(g) △H=。
(2)利用燃烧反应可设计成CO/O2燃料电池(以H2SO4溶液为电解质溶液),写出该电池的正极反应式。
(II)某学生设计了如图所示的装置(框内部分未画出),
在装置内起初发生的反应为Cu+H2SO4H2↑+CuSO4(未注明反应条件),试回答:
(1)该装置的名称是(填“电解池”或“原电池”)。
(2)A、B中至少有一种是金属(填名称),接电源的(填“正极”或“负极”)。
(3)写出该装置中发生还原反应的电极反应方程式为。
(4)若C溶液为100ml饱和食盐水,A 和B电极均为碳棒,该学生利用图示装置进行电解,写出该电解过程中的总反应的离子方程式,当放出标况下112ml氢气时,该溶液的pH=(室温下)。
(III)利用下图装置,可以模拟铁的电化学防护。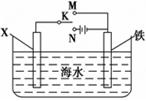
若X为铜,为减缓铁的腐蚀,开关K应置于 处。
若X为锌棒,开关K置于M处,该电化学防护法称为。
氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样
品溶于适量水中,充分搅拌后过滤,再将滤液按下图所示步骤进行操作。
回答下列问题:
(1)试剂Ⅰ的化学式为 ,①中发生反应的离子方程式为 ,;
(2)试剂Ⅱ的化学式为 ,②中加入试剂Ⅱ的目的是 ;
(3)试剂Ⅲ的名称是 ,③中发生反应的离子方程式为 ;
(4)某同学称取提纯的产品0.8000g,溶解后定容在100 mL容量瓶中,每次取25.00 mL溶液,用0.1000 mol·L-1的硝酸银标准溶液滴定,三次滴定消耗标准溶液的平均体积为25.62 mL,该产品的纯度为 。