下列叙述正确的是
| A.浓度均为0.1 mol·L-1的下列溶液,pH由大到小的排列顺序为:NaOH>Na2CO3>(NH4)2SO4>NaHSO4 |
| B.为确定H2A是强酸还是弱酸,可测NaHA溶液的pH,若pH >7,则H2A是弱酸;若pH<7,则H2A是强酸 |
| C.常温下,将pH=3的醋酸溶液稀释到原体积的10倍,稀释后溶液的pH=4 |
| D.常温下KSP(AgCl)=1.5×10-4,此时将足量氯化银固体分别投入相同体积的①蒸馏水②0.1mol/L盐酸③0.1 mol/L氯化镁溶液④0.1 mol/L硝酸银溶液中,则溶液中Ag+浓度:①>④=②>③ |
已知丙酮是一种有机化合物,为无色液体,易溶于水,密度小于1g/cm3,沸点约为55℃,要从丙酮和水的混合物中将丙酮分离出来,下列方法中最合理的是
| A.蒸馏 | B.分液 | C.过滤 | D.结晶 |
关于物质的类别,下列说法正确的是
| A.食盐水、糖水和冰水都是饮料,属于混合物 |
| B.某物质只含有一种元素,则该物质一定是单质 |
| C.烧碱属于碱,纯碱属于盐 |
| D.CuSO4·5H2O是一种混合物 |
下列实验操作中正确的是
| A.不慎将浓碱溶液溅到眼睛里,应立即用大量水冲洗,再涂上硼酸溶液中和 |
| B.从试剂瓶倾倒液体时,试剂瓶标签面向手心 |
| C.用酒精灯直接给烧杯内的液体加热 |
| D.用托盘天平称量5.85g的NaCl |
向60 mL Na2SO4溶液中加入BaCl2溶液,有关数据见下表:
下列有关说法不正确的是
| A.混合前,BaCl2溶液的物质的量浓度为0.10 mol·L-1 |
| B.混合前,Na2SO4溶液的物质的量浓度为0.15 mol·L-1 |
| C.3号实验中沉淀的质量x为1.398 g |
| D.完全沉淀60 mL Na2SO4溶液消耗BaCl2溶液的体积为80 mL |
我国知名企业比亚迪公司开发了具有多项专利的锂钒氧化物二次电池,其成本较低,对环境无污染,能量密度远远高于其他材料电池,电池总反应为V2O5+xLi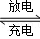 LixV2O5.下列说法中正确的是
LixV2O5.下列说法中正确的是
| A.电池在放电时,Li+向负极移动 |
| B.锂在放电时做正极,充电时为阳极 |
| C.该电池充电时阳极的反应为LixV2O5﹣xe﹣═V2O5+xLi+ |
| D.V2O5只是锂发生反应的载体,不参与电池反应 |