草酸(H2C2O4)是一种重要的有机化工原料。为探究草酸的制取和草酸的性质,进行如下实验。
实验Ⅰ:实验室用硝酸氧化淀粉水解液法制备草酸,装置如下图所示
①一定量的淀粉水解液加入三颈烧瓶中
②控制反应温度55-60℃,边搅拌边缓慢滴加一定量的混合酸(65%的HNO3与98%的H2SO4的质量比2︰1.25)
③反应3小时,冷却,抽滤后再重结晶得到草酸晶体
硝酸氧化淀粉水解液的反应为:
C6H12O6+12HNO3 3H2C2O4+9NO2↑+3NO↑+9H2O
3H2C2O4+9NO2↑+3NO↑+9H2O
(1)上图实验装置中仪器乙的名称为:________________________。装置B的作用是 。
(2)检验淀粉是否水解完全的方法:______________________________________________。实验Ⅱ:探究草酸与酸性高锰酸钾的反应
(3)向草酸溶液中逐滴加入硫酸酸化的高锰酸钾溶液时,可观察到溶液由紫红色变为近乎无色,写出上述反应的离子方程式:____________________________________________________。
(4)学习小组的同学发现,当向草酸溶液中逐滴加入硫酸酸化的高锰酸钾溶液时,溶液褪色总是先慢后快。为探究其原因,同学们做了如下对比实验;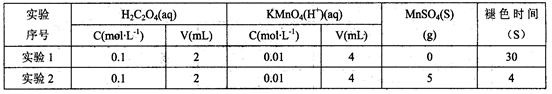
由此你认为溶液褪色总是先慢后快的原因是_________________________________________。
(5)草酸亚铁在工业中有重要作用,草酸可以制备草酸亚铁,步骤如下:
称取FeSO4·7H2O 固体于小烧杯中,加入水和少量稀H2SO4溶液酸化,加热溶解。向此溶液中加入一定量的H2C2O4溶液,将混合溶液加热至沸,不断搅拌,以免暴沸,待有黄色沉淀析出并沉淀后,静置。倾出上清液,再加入少量水,并加热,过滤,充分洗涤沉淀,过滤,用丙酮洗涤固体两次并晾干。
①生成的草酸亚铁需充分洗涤沉淀,检验是否洗涤完全的方法是 。
②用丙酮洗涤固体两次的目的是 。
.(14分) 硫代硫酸钠(Na2S2O3)是常用的还原剂。在维生素C(化学式C6H8O6)的水溶液中加入过量I2溶液,使维生素完全氧化,剩余的I2用Na2S2O3标准溶液滴定,可测定溶液中维生素C的含量。发生的反应为:
C6H8O6+I2===C6H6O6+2H++2I-2S2O32-+I2===S4O62-+2I-
在一定体积的某维生素C溶液中加入1.2molL-1 I2溶液25ml,充分反应后,用1.0molL-1Na2S2O3标准溶液滴定剩余的I2。请回答下列问题:
(1)配制100mL 1.0molL-1 Na2S2O3标准溶液,使用的仪器除天平、药匙、胶头滴管外,还需要___________________________________;配制时,用胶头滴管加水定容至刻度线并盖上瓶塞后的下一步操作是_______________________________________
(2)滴定时,可选择_________________作指示剂。滴定时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_____________________________________。直到出现________________________________________现象为止。
(3)若滴定开始和结束时,滴定管中的液面如图所示。反应消耗Na2S2O3标准溶液的体积是_______________。试根据该实验数据计算该溶液中维生素C的物质的量:mol。
(4)判断下列操作对该溶液中维生素C的物质的量测定结果的影响(填“偏高”、“偏低”或“无影响”)
若在配制标准溶液过程中,烧杯中的Na2S2O3溶液有少量溅出,使测定结果_______;
若在滴定终点读取滴定管刻度时,仰视标准液液面,使测定结果_________
实验室可利用乙醇、铜或铜的化合物制备乙醛,下图是某兴趣小组设计的实验装置,右边的反应装置相同,而左边的气体发生装置不同,试管C中装有水(加热装置未画出)。试回答: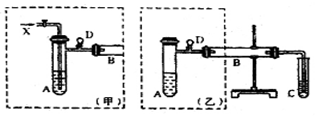
(1)在仪器组装完成后,加装试剂前必须要进行的操作是;
(2)两套装置中的A、B处都需加热,A处用水浴加热,B处用加热,A处用水浴加热的主要优点是。
(3)若按甲装置进行实验,B管处装铜粉,则通入A管的X是,B中反应的化学方程式为。
(4)若按乙装置进行实验,则B管中应装,
B中反应的化学方程式为。
(5)实验结束后,将C试管中的溶液滴入新制的氢氧化铜溶液中并加热,可观察到的
现象,写出该过程的化学方程式。
(2分)下列实验操作或对实验事实的描述中正确的说法有。
①如果苯酚浓溶液沾到皮肤上,应立即用酒精洗涤
②除去甲烷中混有的少量乙烯,可以让混合物通过盛有酸性KMnO4溶液的洗气装置
③实验室制硝基苯:向浓硝酸、浓硫酸的混合酸中滴入苯,在50~60℃的水浴中加热
④实验室制取乙烯时,将无水乙醇和10mol·L-1 H2SO4混合加热到1700C,可制得乙烯
⑤只用溴水就可将苯、四氯化碳、乙醇、己烯四种液体区别开来
⑥检验卤代烃中的卤离子,是将试样放入试管,然后加入NaOH煮沸,随即加入硝酸银即可。
在实验室我们将乙醇、浓硫酸、冰醋酸混合,利用下图所示的装置制取乙酸乙酯。回答下列问题: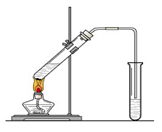
⑴浓硫酸的作用是:①②。
⑵饱和碳酸钠溶液的主要作用是。
⑶装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,其目的是 。
⑷若要把制得的乙酸乙酯分离出来,应采用的实验操作是 。
⑸做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是 。
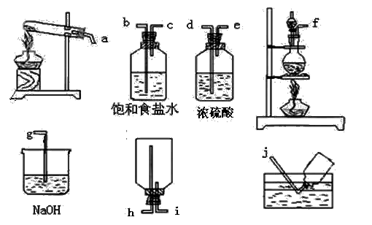
近年来特大地震灾害频繁发生,地震过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。工业上制漂白粉有以下工序:
(1)海水晒盐。
(2)粗盐提纯:粗盐中主要含有MgCl2、Na2SO4和FeCl3杂质,设计如下方案: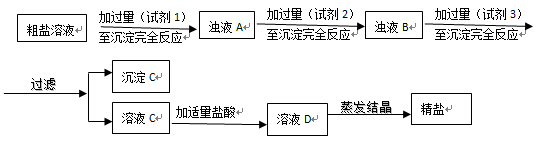
①试剂1~试剂3依次为:..。
②沉淀C含有BaSO4、Mg(OH)2还有(用化学式表示)。
(3)电解法制氯气:观察下图,回答: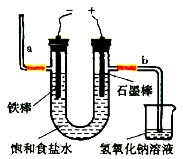
①通电后,(填a或b)侧产生氢气。
②此电解反应的化学方程式为。
(4)制取漂白粉:将氯气通入消石灰(Ca(OH)2)中反应,化学方程式为:。
(5)实验室加热MnO2和浓盐酸混合物来制取氯气。
①若有8.7克的MnO2被还原,则有molHCl被氧化。
②在下列各装置中,选用必要的装置,制备纯净干燥的Cl2,并按从左到右的顺序连接仪器,用接口字母按顺序连接为:。(顺序错误不得分)