FeCl3在现代工业生产中应用广泛。某化学研究性学习小组模拟工业流程制备无水FeCl3,再用副产品FeCl3溶液吸收有毒的H2S。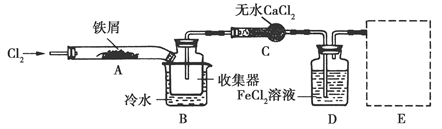
Ⅰ.经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了制备无水FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
①检验装置的气密性;
②通入干燥的Cl2,赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成;
④……
⑤体系冷却后,停止通入Cl2,并用干燥的N2赶尽Cl2,将收集器密封。
请回答下列问题:
(1)装置A中反应的化学方程式为______________。
(2)第③步加热后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管A右端。要使沉积的FeCl3进入收集器,第④步操作是________。
(3)操作步骤中,为防止FeCl3潮解所采取的措施有(填步骤序号)________。
(4)装置B中冷水浴的作用为________;装置C的名称为________;装置D中FeCl2全部反应后,因失去吸收Cl2的作用而失效,写出检验FeCl2是否失效的试剂:________。
(5)在虚线框中画出尾气吸收装置E并注明试剂。
Ⅱ.该组同学用装置D中的副产品FeCl3溶液吸收H2S,得到单质硫;过滤后,再以石墨为电极,在一定条件下电解滤液。
(6)FeCl3与H2S反应的离子方程式为________________。
(7)电解池中H+在阴极放电产生H2,阳极的电极反应式为____________________。
(8)综合分析实验Ⅱ的两个反应,可知该实验有两个显著优点:
①H2S的原子利用率为100%;②________________。
硫酸是化学工业最重要的产品之一,工业制法如下。
(1)生产硫酸最古老的方法是以绿矾为原料,在蒸馏釜中煅烧。反应的化学方程式为:2FeSO4·7H2O Fe2O3+SO2+SO3↑+14H2O。其中三氧化硫与水蒸气同时冷凝便得到硫酸。用如图所示装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫(加热装置已略去)。其中b为干燥的试管
Fe2O3+SO2+SO3↑+14H2O。其中三氧化硫与水蒸气同时冷凝便得到硫酸。用如图所示装置模拟用绿矾制硫酸的实验,并检验生成的硫酸和二氧化硫(加热装置已略去)。其中b为干燥的试管 。
。
①试管b中得到的主要产物是,检验该产物的方法是(结合离子方程式简要说明)。
②为检验反应的另一种生成物,试管c中应加入的试剂是,简述相应的实验现象及结论。
③所得硫酸的理论浓度(溶质的质量分数)为。
(2)目前,我国采用“接触法”制硫酸,生产设备如图所示:
①图中设备A的名称是,a、b两处所含气体的化学式分别为、。
②有关接触法制硫酸的下列说法中,不正确的是。
| A.二氧化硫的接触氧化在合成塔中发生 |
| B.吸收塔得到的硫酸浓度为98% |
| C.煅烧含硫48%的黄铁矿时,若FeS2损失了2%,则S损失4% |
D. B装置中反应的条件之一为较高温度是为了提高SO2的转化率 B装置中反应的条件之一为较高温度是为了提高SO2的转化率 |
(3)随着化学工业的发展,“接触法”全面替代了“绿矾热分解法”,请你从综合效益的角度指出“接触法”制硫酸的优势:①生产成本低、②原料易得、③、④ 、⑤、⑥(可不填满)。
、⑤、⑥(可不填满)。
(16分)、据《中国制药》报道,化合物F是用于制备“非典”药品(盐酸祛炎痛)的中间产物,其合成路线为:
已知:一定条件(Ⅰ)RNH2+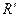 CH2Cl→ RNHCH2
CH2Cl→ RNHCH2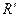 +HCl(R和
+HCl(R和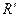 代表烃基);
代表烃基);
(Ⅱ)苯的同系物能被酸性高锰酸钾溶液氧化,如:
(Ⅲ) (苯胺,弱碱性,易氧化)
(苯胺,弱碱性,易氧化)
(Ⅳ)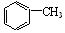 与浓硫酸、浓硝酸混合在不同温度下会得到不同产物
与浓硫酸、浓硝酸混合在不同温度下会得到不同产物
回答下列问题:
(1)C的结构简式是 。
(2)请写出D+E→F的化学方程式: 。
(3)E在一定条件下,可聚合成很好的功能高分子材料,写出合成此高聚物的化学方程式 。
(4)反应①~⑤中,属于取代反应的 是(填反应序号)
是(填反应序号)
(5)符合下列条件的E的同分异构体的数目是()。
①与FeCl3溶液有显色反应②能发生银镜反应③苯环上的一溴取代物只有3种。
| A.3种 | B.8种 | C.10种 | D.12种 |
(6) 已知苯甲醛在一定条件下可以通过Perkin反应生成肉桂酸(产率45~50%),反应方程式如下:
C6H5CHO + (CH3CO)2O → C6H5CH="CHCOOH" +CH3COOH
苯甲醛肉桂酸
若苯甲醛的苯环上有取代基,也能发生Perkin反应,相应产物的产率如下:
反应物 |
 |
|||
| 产率(%) |
15 |
23 |
33 |
0 |
反应物 |
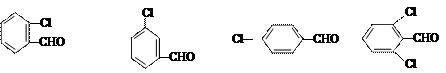 |
|||
| 产率(%) |
71 |
63 |
52 |
82 |
请根据上表回答:取代基对Perkin反应的影响有(写出3条即可):
①
②
③ [来
为了研究铜与硝酸的反应,化学兴趣小组设计了如下实验装置,其中a、b、c是活塞。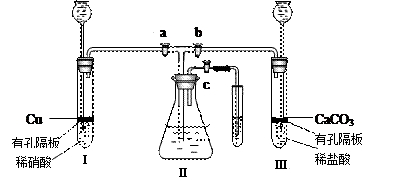
(1)装药品前,按图装置连接后,如何检验气密性?
(2)按
图装药品后,如果开启 a 和 c ,关闭b ,则Ⅱ中的现象是
;若要使Ⅱ里的气体始终保持无色,应该怎样操作?
写出Ⅰ及Ⅱ中发生的反应的离子方程式:
(3)如果将Ⅰ管中的稀硝酸换成浓硝酸,开启 a 和 c ,关闭 b ,过一会观察,可以看到Ⅱ里没入水中的导管有气泡冒出,导管内气体呈红棕色,液面上方气体为无色,试用文字及方程式解释这一现象 。
。
(4)在实验(2)中,如果装置Ⅰ、Ⅱ里液面上空间的总体积为Vml,空气中氧气的体积分数为 21%,实验在标准状况下进行,全部氧气通过反应转化为硝酸;实验开始时加入的铜为mg,实验完毕后剩余铜ng,Ⅱ中所得溶液的体积也为Vml(不考虑装置外空气的可能进入)。则Ⅱ中所得溶液的物质的量浓度是。
W、X、Y、Z是短周期中的四种常见元素,其原子序数依次增大。W、Y的氧化物是导致酸雨的主要物质,X原子最外层电子数等于电子层数,Z元素的最高价氧化物的水化物的酸性是最强的。
(1)W位于元素周期表第______周期第______族。W的气态氢化物稳定性比 ______(填“强”或“弱”)。
______(填“强”或“弱”)。
(2)Y有两种常见的氧化物,能同时使溴水和酸性高锰酸钾溶液褪色的是(写化学式),并写出这两个离子方程式:
_______________________________________________________________________
________________________________________________________________________
(3) 实验室制取Z的单质的化学方程式是:_______________________________________。
实验室制取Z的单质的化学方程式是:_______________________________________。



X的单质和FeO反应的热化学方程式是_________________________________________。
为测定某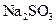 样品(含少量
样品(含少量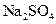 杂质)的纯度,实验室按以下步骤进行:①称取
杂质)的纯度,实验室按以下步骤进行:①称取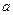
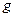 样品,置于烧杯中;
样品,置于烧杯中;
②加入适量蒸馏水,使样品溶解,然后配制成250mL溶液;
③准确量取25.00mL步骤②中配得的溶液;
然后,可采用下列两种方法进行测定:
| 方法一 |
方法二 |
| ④将25.00mL溶液置于烧杯中,加入过量的稀盐酸充分搅拌; ⑤加入过量 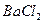 溶液,充分搅拌,使沉淀完全; 溶液,充分搅拌,使沉淀完全;⑥过滤、洗涤、干燥沉淀、称量得到bg固体。 |
④将25.00mL溶液置于锥形瓶中; ⑤用0.1 mol 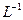 的酸性 的酸性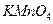 溶液进行滴定,达到滴定终点时,消耗10.00mL溶液。 溶液进行滴定,达到滴定终点时,消耗10.00mL溶液。 |
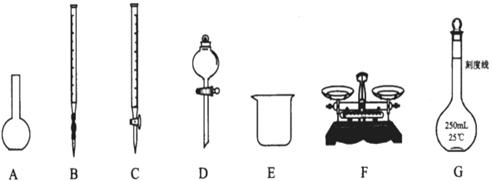
请根据上述实验,回答:
(1)上图所示仪器中,本实验步骤①②③中必须用的的仪器是E和_______(填字母);
(2)在方法一④中加入过量稀盐酸的目的是____________________________________;
(3)在方法一测定得到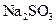 样品的纯度是______________(列出算式,可不化简);
样品的纯度是______________(列出算式,可不化简);
(4)在方法二中,是否需要加入指示剂________(填“是”或“否”),请简述理由___
____________________________ ______________________________________;
______________________________________;
(5)在方法二中达到滴定终点读取数据时,俯视液面,则测定结果___________________(填“偏高”、“偏低”、“无影响”)。