A~G是前四周期除稀有气体之外原子序数依次增大的七种元素。A与其他元素既不同周期又不同族;B、C的价电子层中未成对电子数都是2;E核外的s、p能级的电子总数相等;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满。回答下列问题:
(1)写出元素名称:B ,G 。
(2)写出F的价电子排布图: 。
(3)写出化合物BC的结构式: 。
(4)由A、C、F三元素形成的离子[F(CA)4]— 是F在水溶液中的一种存在形式,其中F的杂化类型是 。
(5)在测定A、D形成的化合物的相对分子质量时,实验测定值一般高于理论值的主要原因是 。
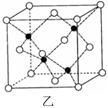
(6)E的一种晶体结构如图甲,则其一个晶胞中含有 个E;G与D形成的化合物的晶胞结构如图乙,若晶体密度为ag/cm3,则G与D最近的距离为 pm
(阿伏加德罗常数用NA表示,列出计算表达式,不用化简;乙中○为G,●为D。)
(1) 用系统命法写出下列物质名称或结构简式
2,2,3-三甲基丁烷的结构简式是
画出3-甲基-1-丁烯的键线式。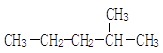 的系统命名是:
的系统命名是:
(2)写出下列反应的化学方程式
苯的硝化反应
乙烯发生加聚反应
乙醛与新制氢氧化铜反应
(1)下列各组化合物中,属于同系物的是(填入编号),属于同分异构体的是(填入编号)。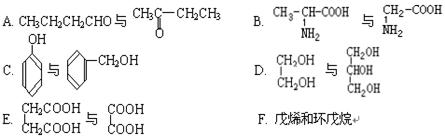
(2)有机物A: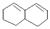 在加热条件下和Br2 按物质的量之比1:1发生的非邻位碳的加成反应
在加热条件下和Br2 按物质的量之比1:1发生的非邻位碳的加成反应
方程式
(3)某高分子有机物 是由一种单体缩聚而成的,该单体的结构简式为。
是由一种单体缩聚而成的,该单体的结构简式为。
金银花是治疗和预防甲型H1N1的常见中草药,有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构式见图,下列有关绿原酸的说法不正确的是()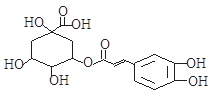
| A.分子式为C16H18O9 |
| B.1mol绿原酸与溴水反应最多消耗4molBr2 |
| C.1mol绿原酸最多与5molH2加成 |
| D.1mol绿原酸最多与4molNaOH反应 |
下列离子方程式不正确的是()
A.溴乙烷在氢氧化钠水溶液中的反应:CH3CH2Br + OH-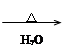 CH3CH2OH +Br- CH3CH2OH +Br- |
B.醋酸溶液与氢氧化铜反应:2CH3COOH + Cu(OH)2 Cu2+ + 2CH3COO-+ 2H2O Cu2+ + 2CH3COO-+ 2H2O |
C.苯酚钠溶液中通入少量二氧化碳:2C6H5O-+ CO2 + H2O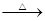 2C6H5OH + CO32- 2C6H5OH + CO32- |
| D.甲醛溶液与足量的银氨溶液共热 |
HCHO+4[Ag(NH3)2]++4OH-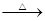 CO32-+2NH4+ +4Ag↓+6NH3+2H2O
CO32-+2NH4+ +4Ag↓+6NH3+2H2O
(8分)【化学——物质结构与性质】A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为_______;
(2)B元素的负一价离子的电子层结构与氩相同,C元素的正一价禽子的电子层结构与氙相同,B、C形成的化合物的化学式为________;其晶体内每个B离子周围有_____个C离子与之紧相邻。其晶体的主要物理性质有:___________________________________(写出两条即可)。
(3)D元素的正三价离子的3d亚层为半充满,D的元素符号为______,其基态原子的电
子排布式为___________________________________。
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其单质在一定条件下能与硫(S)反应,试写出该反应方程式 _____________________________。