X、Y、Z三种主族元素的单质在常温下都是常见的无色气体,在适当条件下,三者之间可以两两发生反应生成分别是双核、三核和四核的甲、乙、丙三种分子,且乙、丙分子中含有X元素的原子个数比为2∶3。请回答下列问题:
(1)元素X的名称是________,丙分子的电子式为________。
(2)若甲与Y单质在常温下混合就有明显现象,则甲的化学式为________。丙在一定条件下转化为甲和乙的反应方程式为___________________________。
(3)化合物丁含X、Y、Z三种元素,丁是一种常见的强酸,将丁与丙按物质的量之比1∶1混合后所得物质戊的晶体结构中含有的化学键为________(选填序号)。
a.只含共价键 b.只含离子键 c.既含离子键,又含共价键
氮化硅(Si3N4)是一种新型陶瓷材料,它可在高温下的氮气流中由石英与焦炭通过以下反应制得:3SiO2(s) + 6C(s) + 2N2(g) Si3N4(s) + 6CO(g) + Q(Q>0)
Si3N4(s) + 6CO(g) + Q(Q>0)
完成下列填空:
(1)某温度下该反应在一容积为2L的密闭容器中进行,2min后达到平衡,刚好有2mol电子发生转移,则2min内反应的速率为:v(CO) = ;该反应的平衡常数表达式为 。
(2)其它条件不变时仅增大压强,则。
a.K值减小,平衡向逆反应方向移动
b.K值增大,平衡向正反应方向移动
c.K值不变,平衡向逆反应方向移动
d.K值不变,平衡向正反应方向移动
(3)一定条件下能说明上述反应已达平衡的是 。
a.c(N2 ) : c(CO) = 1:3 b.3v(N2 ) = v(CO)
c.固体质量不再改变 d.气体密度不再改变
达到平衡后改变某一条件,反应速率v与时间t的关系如图所示。
若不改变N2与CO的量,则图中t4时引起变化的原因可能是 ;图中t6时引起变化的原因可能是。
由图可知,平衡混合物中CO含量最高的时间段是。
铬及其化合物常被应用于冶金、化工、电镀、制药、纺织等行业,但使用后的废水因其中含高价铬的化合物而毒性很强。工业上往往采取下列循环工艺防止铬的污染: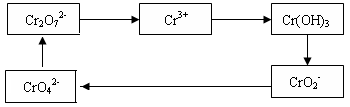
完成下列填空:
(1)含Cr2O72-离子的废水在酸性条件下用Fe3O4处理,反应的离子方程式如下:
Cr2O72- +Fe3O4 +H+ →Cr3+ +Fe3+ +H2O
配平上述离子反应方程式,并标出反应中电子转移的方向和数目。
(2)向上述反应后的溶液中加入碱溶液,让废水的pH升至8~10,控制适当的温度,使产物中的金属阳离子全部转变为沉淀。写出从该沉淀中分离出Cr(OH)3的离子方程式、
。
(3)回收所得的Cr(OH)3,经处理后又可转变成K2Cr2O7。纯净的K2Cr2O7常用于准确测定Na2S2O3溶液的物质的量浓度,方法如下:
① Cr2O72- +6I- + 14H+ →3I2 + 2Cr3+ + 7H2O② 2S2O32- + I2→S4O62- + 2I-
准确称取纯净的K2Cr2O7 0.1225g ,配成溶液,用Na2S2O3溶液滴定,消耗Na2S2O3溶液25.00mL。则Na2S2O3溶液的物质的量浓度为(保留四位有效数字)。
香豆素是广泛存在于植物中的一类芳香族化合物,大多具有光敏性,有的还具有抗菌和消炎作用。它的核心结构是芳香内酯A,其分子式为C9H6O2。该芳香内酯A经下列步骤转变为水杨酸、乙二酸等物质。 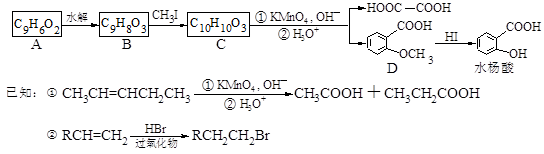
(1)写出化合物A的结构简式_____________________。
(1)上述转化过程中,属于取代反应的有____个;反应步骤B→C的目的是______________。
(1)化合物D有多种同分异构体,其中一类同分异构体是苯的二取代物,且水解后生成的产物之一能发生银镜反应。这类同分异构体(不含C-O-O-结构)共有_____种。
(1)鉴别A、B、C三种物质,所需的试剂是________(选填编号)。
a.饱和FeCl3溶液,新制Cu(OH)2悬浊液 b.饱和FeCl3溶液,酸性KMnO4溶液
c.饱和FeCl3溶液,NaOH溶液d.饱和FeCl3溶液,饱和NaHCO3溶液
(1)设计合理方案,由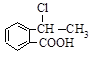 合成
合成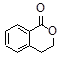 ,写出相关化学反应方程式。
,写出相关化学反应方程式。
某芳香烃X(相对分子质量为92)是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H是一种功能高分子,链节组成为(C7H5NO)。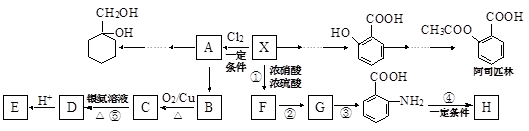
已知: (苯胺,易被氧化)
(苯胺,易被氧化)
完成下列填空:
(1)X的结构简式是,反应⑤的类型是。
(2)反应②③两步能否互换(填“能”或“不能”),理由是____________________。
(3)反应④的化学方程式是。
(4)检验B是否完全转化为C的方法是(选填编号)。
a.定量分析:测熔点 b.定性分析:酸性高锰酸钾溶液
c.定量分析:银氨溶液 d.定性分析:新制氢氧化铜
联碱法(候氏制碱法)和氨碱法的生产流程简要表示如下图:
(1)两种方法的沉淀池中均发生的反应化学方程式为_____________________________。
(2)若沉淀池含800.00 mol NH3的水溶液质量为54.00 kg,向该溶液通入二氧化碳至反应完全,过滤,得到滤液31.20kg,则NH4HCO3的产率为______________%。
(3)在氨碱法生产过程中氨要循环使用,但不需要补充,在母液中加生石灰前先要加热的原因是 ___ 。
(4)根据联碱法中从滤液中提取氯化铵晶体的过程推测,所得结论正确是_______(选填编号)。
a.常温时氯化铵的溶解度比氯化钠小
b.通入氨气能增大NH4+的浓度,使氯化铵更多析出
c.加入食盐细粉能提高Na+的浓度, 使NaHCO3结晶析出
d.通入氨气能使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
(5)联碱法相比于氨碱法,氯化钠利用率从70%提高到90%以上,主要是设计了循环Ⅰ,联碱法的另一项优点是__________________________________________________。
(6)从沉淀池析出的晶体含有NaCl杂质,某同学在测定其NaHCO3的含量时,称取5.000g试样,配制成100mL溶液,用标准盐酸溶液滴定(用甲基橙做指示剂),测定数据记录如下:
| 滴定次数 |
待测液(mL) |
0.6000mol/L盐酸溶液的体积(mL) |
|
| 初读数 |
终读数 |
||
| 第一次 |
20.00 |
1.00 |
21.00 |
| 第二次 |
20.00 |
如右图Ⅰ |
如右图Ⅱ |
①第二次滴定,从图Ⅰ图Ⅱ 显示消耗的盐酸溶液体积为。
显示消耗的盐酸溶液体积为。
②该实验测定NaHCO3含量的计算式为ω(NaHCO3)=。
③该同学测定结果有一定的误差,产生该误差的原因可能是(选填编号)。
a.待测液中加入甲基橙作指示剂,用标准酸液滴定至变橙色
b.锥形瓶用蒸馏水洗涤后,直接加入待测溶液进行滴定
c.滴定管用蒸馏水洗涤后,直接注入标准酸液进行滴定
d.滴定管用蒸馏水洗涤后,直接注入待测液,取20.00 mL进行滴定