在一定温度下,发生如下反应:N2(g)+3H2(g)  2NH3(g),起始时,充入的N2和H2的物质的量分别是3.0 mol和6.0 mol,平衡时生成NH3的物质的量是2.4 mol。已知容器的容积为5.0 L,试求:
2NH3(g),起始时,充入的N2和H2的物质的量分别是3.0 mol和6.0 mol,平衡时生成NH3的物质的量是2.4 mol。已知容器的容积为5.0 L,试求:
(1)H2的转化率是________。
(2)平衡时混合气体中N2的体积分数是________。
下表是元素周期表中短周期元素部分,表中字母分别代表一种元素:
| a |
b |
||||||
| d |
e |
f |
|||||
| c |
g |
h |
(1)上述 元素(填元素名称)可以形成硬度最大的单质。
(2)“神舟”六号飞船内需要有一种化合物来吸收宇航员呼出的 CO2,并释放出O2,你认为该
物质应该是由上表中的 和 元素(填元素名称)组成的。飞船中需要制造一种适合宇航员生存的人工生态环境,应该在氧气中充入一种气体用于稀释氧气,该气体分子是 。
(3)表中元素g的氢化物稳定性比元素e的氢化物的稳定性 (填“强”或“弱”)。
(4)将潮湿的由h元素构成的单质通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色。则甲装置中所盛试剂可能是
|
①浓硫酸②NaOH溶液③KI溶液④饱和食盐水
(5)写出h元素构成的单质与水反应的化学方程式: 。在原子序数1—18号元素中,按要求用合适的化学用语填空:
(1)与水反应最剧烈的金属是_____________。
(2)与水反应最剧烈的非金属单质是_____________。
(3)原子半径最小的元素是______________。
(4)最稳定气态氢化物的化学式是______________。
(5)最高价氧化物对应水化物的酸性最强的化学式是_______________。
(6)电子数为10的化合物分子式__、__、__、__。
(共10分)有下列各组物质:
| A.O2和O3(臭氧) |
B. 和 和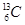 |
C.CH3CH2CH2CH3和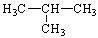 |
D.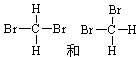 |
E.甲烷和庚烷
F.(CH3)2CH2与C(CH3)4
G.金刚石和石墨
H.液氯与氯气
(1)组两物质互为同位素(2)组两物质互为同素异形体
(3)组两物质属于同系物(4)组两组物质互为同分异构体
(5)组中的物质是同一物质
常温下将0.01molCH3COONa和0.004mol盐酸溶于水,配成0.5L混合溶液。
(1)溶液中共有________种微粒。
(2)溶液中有两种微粒的物质的量之和一定等于0.01mol,它们是____________。
(3)溶液中n(CH3COO-)+n(OH-)-n(H+)=_________mol。
在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才能发生化学反应。能引发化学反应的碰撞称之为有效碰撞,这些分子称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位用kJ•mol-1表示。请认真观察下图,然后回答问题。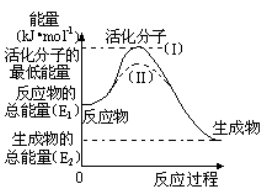
(1)图中反应是(填“吸热”或“放热”)反应,该反应(填“需要”或“不需要”)提供能量,该反应的△H=(用含E1、E2的代数式表示)。
(2)已知热化学方程式:H2(g)+1/2O2(g) ===H2O(g)△H=-241.8kJ•mol-1,该反应的活化能为167.2 kJ•mol-1,则其逆反应的活化能为。
(3)对于同一反应,图中虚线(II)与实线(I)相比,活化能大大降低,活化分子的百分数增多,反应速率加快,你认为最可能的原因是。