氯化铬酰(CrO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。
请回答下列问题:
(1)写出铬原子的基态电子排布式________,与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有________(填元素符号),其中一种金属的晶胞结构如图所示,该晶胞中含有金属原子的数目为________。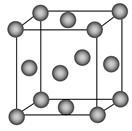
(2)CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是________(填“极性”或“非极性”)分子。
(3)在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有________(填序号),CS2分子的空间构型是________。
判断物质中化学键时应该注意一些问题,下列说法中正确的是
①存在离子键的化合物一定是离子化合物,离子化合物中一定存在离子键
②离子化合物可以只含非金属元素,也可以存在共价键,如NH4Cl
③共价化合物中只含有共价键,不含离子键
④非金属单质(稀有气体除外)中只含有共价键
⑤稀有气体由单原子组成,无化学键
⑥只含有共价键的化合物一定是共价化合物,只含有共价键的物质不一定是共价化合物,可能是单质;含有共价键的化合物不一定是共价化合物,可能是离子化合物,例如NaOH
画出下列短周期元素的原子结构示意图:
(1)质量数为23,中子数为12的原子
(2)最外层电子数是次外层电子数3倍的原子
发生化学反应时,破坏化学键需要能量,形成化学键需要能量。吸收能量用E1表示,释放能量用E2表示,当E1E2时,反应吸收能量;当E1E2时,反应释放能量
工业上以粗铜为原料采取如图所示流程制备硝酸铜晶体: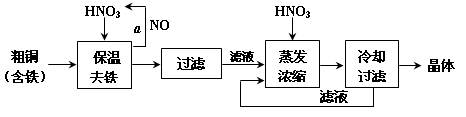
(1)在步骤a中,还需要通入氧气和水,发生反应的化学方程式是
。
(2)在保温去铁的过程中,为使Fe3+沉淀完全,可以向溶液中加入CuO,调节溶液的pH,根据下表数据,溶液的pH应保持在范围。若调节溶液的pH=4,此时,溶液中c (Fe3+) =。[已知该条件下,Fe(OH)3的KSP= 4.0×10-36 ]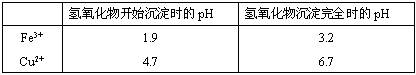
(3)不用加水的方法调节溶液pH的原因是。
(4)进行蒸发浓缩时,要加适量的硝酸以保持溶液一定的c(H+),其目的是(结合离子方程式简要说明)。
(5)工业上常利用硝酸铜溶液电镀铜,电镀时阴极的电极反应式是。
[化学——有机化学基础]
Ⅰ.对羟基肉桂酸是一种强效的导电材料,在液晶显示器工业中近年来研究广泛。结构简式如图。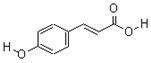
(1)该有机物具有的官能团名称是(写出其中的两种)。
(2)该有机物能发生的反应类型是(填写代号)。
A.氧化反应 B.消去反应 C.加聚反应 D.水解反应
Ⅱ.芳香族化合物C10H10O2有如下的转化关系: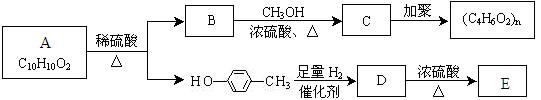
已知E能使Br2/CCl4溶液褪色。请回答下列问题:
(3)请分别写出A、E的结构简式A E。
(4)若有机物F与C互为同分异构体,则与有机物B为同系物的F的同分异构体有种
(5)请写出B→C反应的化学方程式。