海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下: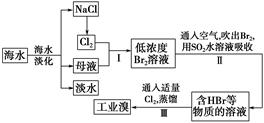
(1)请列举海水淡化的两种方法:________、________。
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是_________。
(3)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为_______,
由此反应可知,除环境保护外,在工业生产中应解决的主要问题是_______。
(4)某化学研究性学习小组为了了解从工业溴中提纯溴的方法,查阅了有关资料知:Br2的沸点为59 ℃,微溶于水,有毒并有强腐蚀性。他们参观生产过程后,画了如下装置简图: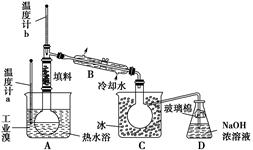
请你参与分析讨论:
①图中仪器B的名称是____________。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是__________。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件?___________。
④C中液体颜色为________________。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是________________。
现有阳离子交换膜、阴离子交换膜、石墨电极,请用氯碱工业中的膜技术原理,回答下列问题。
(1)写出氯碱工业中电解饱和食盐水的反应式________________,阳离子交换膜在氯碱工业中的作用是____________________________________________。写出用惰性电极电解硫酸钠水溶液的总反应式:____________________________________________。
(2)请利用交换膜技术,根据上图框架,设计一个电解硫酸钠溶液制氢氧化钠溶液和硫酸溶液的装置,标出进出物质的名称。A___________;B___________;C___________;D___________;E___________;F___________;G___________。膜b为___________(填“阳离子交换膜”或“阴离子交换膜”)。
用下图所示的装置进行电解。通电一会儿,发现湿润的KI淀粉试纸的C端变为蓝色。则: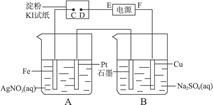
(1)A中发生反应的化学方程式为_________________________________。
(2)在B中观察到的现象是__________________________、______________________、______________________。
(3)室温下,若从电解开始到时间t s时,A、B装置中共收集到标准状况下的气体0.168 L,若电解过程中无其他副反应发生,经测定电解后A中溶液体积恰为1000 mL,则A溶液的pH为______________________。
(1)阿波罗宇宙飞船使用的是以KOH为介质的氢、氧燃料电池(如下图),按下列要求填空: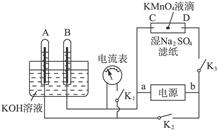
(1)①__________(填“负”或“阴”)极反应式:;②__________(填“正”或“阳”)极反应式:_________________;③电池反应式_________________________________。
(2)如图所示装置,A、B中的电极为多孔的惰性电极;C、D为夹在湿的Na2SO4滤纸条上的铂夹;电源有a、b两极。若A、B中充满KOH溶液后倒立于KOH溶液的水槽中,切断K1,闭合K2、K3通直流电,回答下列问题:
①判断电源的正、负极:a为___________极,b为极___________。
②在湿的Na2SO4溶液滤纸条中心的KMnO4液滴,有什么现象?______________________。
③写出电极反应式:A极______________________,C极______________________。
④若A极产生气体的体积在标准状况下为x L,则C极上产物的质量大约为___________g。
⑤若电解一段时间后,A、B中均有气体包围电极,此时切断K2、K3,闭合K1,则电流表的指针是否移动___________(填“是”或“否”)。若电流表指针不移动说明理由,若指针移动也说明理由。
如下图所示,若电解5 min铜电极质量增加2.16 g。试回答: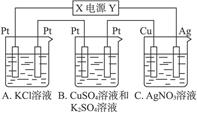
(1)电极X是电源的___________极。
(2)pH变化:A___________;B___________;C___________。
(3)若A中KCl溶液的体积为200 mL,电解至5 min溶液的pH是__________(假设溶液体积不变化)。
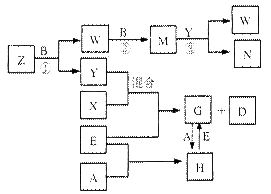 A、B、C、D、E是中学化学常见的五种单质,已知A、B、C、D在常温下均为气态,E为金属,其中D能分别跟A、B、C在一定条件下化合,生成对应的化合物X、Y、Z,其中常温下,Y为液体,X、Z为气体。有关的转化关系如下图所示(反应条件均已略去)。
A、B、C、D、E是中学化学常见的五种单质,已知A、B、C、D在常温下均为气态,E为金属,其中D能分别跟A、B、C在一定条件下化合,生成对应的化合物X、Y、Z,其中常温下,Y为液体,X、Z为气体。有关的转化关系如下图所示(反应条件均已略去)。
(1)化合物Z的空间构型为;构成A的元素的最高价氧化物水化物的化学式为;实验室贮存N的方法是。
(2)写出反应②的化学反应方程式;G→H的离子方程式。
(3)常温下,D与A反应生成1 mol X时放热92.3kJ,写出该反应的热化学方程式:
。
(4)将过量的E加入N的稀溶液中,若反应过程中转移电子的数目为3.01×1023,则参加反应的E的质量为g。