(1)火山喷发所产生的硫磺可用于生产重要的化工原料硫酸。某企业用下图所示的工艺流程生产硫酸:
请回答下列问题:
①为充分利用反应放出的热量,接触室中应安装________(填设备名称)。吸收塔中填充有许多瓷管,其作用是_______________________。
②为使硫磺充分燃烧,经流量计1通入燃烧室的氧气过量50%。为提高SO2转化率,经流量计2的氧气量为接触室中二氧化硫完全氧化时理论需氧量的2.5倍,则生产过程中流经流量计1和流量计2的空气体积比应为________。假设接触室中SO2的转化率为95%,b管排出的尾气中二氧化硫的体积分数为________(空气中氧气的体积分数按0.2计),该尾气的处理方法是________。
③与以黄铁矿为原料的生产工艺相比,该工艺的特点是________(可多选)。
A.耗氧量减少
B.二氧化硫的转化率提高
C.生产的废渣减少
D.不需要使用催化剂
(2)硫酸的用途非常广泛,可应用于下列哪些方面________(可多选)。
A.橡胶的硫化
B.表面活性剂“烷基苯磺酸钠”的合成
C.铅蓄电池的生产
D.过磷酸钙的制备
(3)矿物燃料的燃烧是产生大气中SO2的主要原因之一。在燃煤中加入适量的石灰石,可有效减少煤燃烧时SO2的排放,请写出此脱硫过程中反应的化学方程式___________________________________________________________。
向含有1.6 g KBr的溶液中加入含杂质Cl2的粗溴6.0 g,烘干得残留固体1.3 g,则粗溴中氯的质量分数为______________。
通常状况下,
、
和
是三种气态单质。X的组成元素是第三周期原子半径最小的元素(稀有气体元素除外);Y和Z均由元素R组成,反应
常作为Y的鉴定反应。
(1)
与
的关系是(选填字母)。
a.同位素 b.同系物
c.同素异形体 d.同分异构体
(2)将
和二氧化硫分别通入品红溶液,都能使品红褪色。简述用褪色的溶液区别二者的实验方法:。
(3)举出实例说明
的氧化性比硫单质的氧化性强(用化学方程式表示):。
(4)气体
与
化学性质相似,也能与
反应生成
(其水溶液是一种酸)。
①
分子中含有4个共价键,其结构式是。
②
溶液显碱性,原因是(用离子方程式表示)。
(5)加热条件下,足量的
与某金属M的盐
(
为碳元素)完全反应生成
和
(
、
均为正整数)。若
质量为
,
质量为
,M的相对原子质量为
,则
中
∶
=(用含
、
和
的代数式表示)。
根据下图的转化关系完成下列有关问题。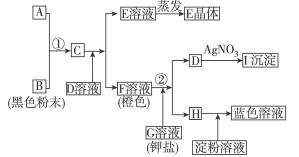
(1)写出①的离子方程式______________________________________;
写出②的离子方程式________________________________________。
(2)写出下列物质或溶液中溶质的化学式。
E_______________________________________,I____________________________________。
(3)在上述转化过程中,判断B、C、F、H氧化能力由弱到强的顺序(写化学式):
_______________________________________________________________________________。
已知甲、乙、丙为常见单质,A、B、C、D、X、Y、Z为常见的化合物,Y的摩尔质量数值比Z的小16,乙、丙的摩尔质量相同,B的摩尔质量比D的小2,B、X的摩尔质量相同,各物质转化关系如下:
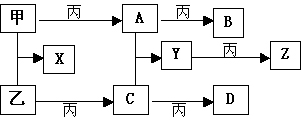 |
1、写出下列有关物质化学式:丙_________;B _________。
2、写出Y→Z反应化学方程式__________________________。
A、B、C、D四种元素原子核电荷数依次增大(均小于20),其单质及相应的化合物能发生如下反应关系:
 |
1.写出B、D形成化合物电子式__________________。
2.写出下列有关物质化学式:E ___________, J _____________。
3.写出C单质与H水溶液反应的离子方程式___________________。