工业碳酸钠(纯度约为98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42-等杂质,提纯工艺线路如下: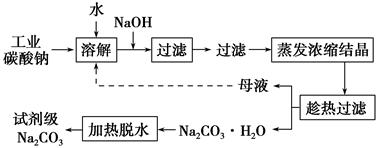
Ⅰ.碳酸钠的饱和溶液在不同温度下析出的溶质如图所示:
Ⅱ.有关物质的溶度积如下:
| 物质 |
CaCO3 |
MgCO3 |
Ca(OH)2 |
Mg(OH)2 |
Fe(OH)3 |
| Ksp |
4.96×10-9 |
6.82×10-6 |
4.68×10-6 |
5.61×10-12 |
2.64×10-39 |
回答下列问题:
(1)加入NaOH溶液时发生反应的离子方程式为:_____________________________________。
向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Fe3+)=________。
(2)“趁热过滤”时的温度应控制在________。
(3)有人从“绿色化学”角度设想将“母液”沿流程中虚线所示进行循环使用。请你分析实际工业生产中是否可行________,并说明理由________________________________________。
(4)已知:Na2CO3·10H2O(s)=Na2CO3(s)+10H2O(g) ΔH=+532.36 kJ·mol-1
Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H2O(g)ΔH=+473.63 kJ·mol-1
写出NaCO3·H2O脱水反应的热化学方程式________________________________________。
物质A~E都是由下表中离子组成的,常温下各物质从1mL稀释到1000mL,pH的变化如图甲所示,其中A与D反应得到E。请回答:
| 阳离子 |
NH4+、H+、Na+ |
| 阴离子 |
OH-、CH3COO-、Cl- |

(1)根据pH的变化关系图甲,写出物质的化学式:B:,D:。
(2)图甲a>9的理由是
(3)另取浓度为C1的B溶液25mL,向其中逐滴滴加0.2mol/L的D溶液,滴定过程中溶液pH的变化曲线如乙图所示。
①C1为;
②G点溶液呈中性则滴加入D溶液的体积V12.5mL(填>,<或=)
③常温下B、C溶液的pH分别是a、b且a+b=13则将B、C混和恰好完全 反应时所消耗B、C溶液的体积比VB:VC=
反应时所消耗B、C溶液的体积比VB:VC=
J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如下表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的元素。
(1)元素T的名称是
(2)J和氢元素组成的化合物A每个分子由4个原子组成,已知充分燃烧a gA物质时生成1mol二氧化碳气体和液态水,并放出热量b kJ,则A物质燃烧热的热化学方程式是
(3)工业燃烧焦炭后的尾气中含有M和R组成的气体,为了测定其含量,可以选择的试剂是
| A.氢氧化钠溶液 | B.硫酸酸化的高锰酸钾溶液 | C.淀粉碘化钾溶液 | D.溴水溶液 |
(4)在微电子工业中,L的最简单气态氢化物的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为:
(5)由L和M组成的 两种价态相同的气体化合物可以相互转化,在同温同容的甲乙容器中分别加入1mol和2mol的LM2气体,分别建立平衡,则两容器中LM2的转化率比较甲乙(<,>,=)
两种价态相同的气体化合物可以相互转化,在同温同容的甲乙容器中分别加入1mol和2mol的LM2气体,分别建立平衡,则两容器中LM2的转化率比较甲乙(<,>,=)
(6)与J同主族的另一短周期元素和M组成的化合物有很广泛的用途,请说出其主要应用,写出两种
现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题。(由实验装 置引起的实验误差忽略不计)。
置引起的实验误差忽略不计)。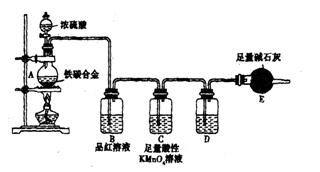
Ⅰ.探究 浓硫酸的某些性质
浓硫酸的某些性质
(1)称量E的质量;按照图示连续装置,检查装置的气密性。
(2)将mg铁碳合金样品放入A中,再加入适量的浓硫酸。未点燃酒精灯前,A、B均无明显现象,其原因是:。点燃酒精灯一段时间后,B中可观察到的明显现象是。
C中足量的酸性KMnO4溶液所起的作用是。D中盛放的试剂是。
(3)反应一段时间后,从A中逸出气体的速率仍然较快,除因反应温度较高外,还可能的原因是。
Ⅱ.测定铁的质量分数
(4)待A中不再逸出气体时,停止加热,拆下E并称重,E增重bg,则铁碳合金中铁的质量分数为(写表达式)。某同学认为:依据此实验测得的数据,计算合金中铁的质量 分数可能会偏低,你认为可能的原因是。
分数可能会偏低,你认为可能的原因是。
(5)经过大家的讨论,决定采用右图装置和其他常用实验仪器测定某些数据即可,为了快速和准确地计算出铁的质量分数,最简便的实验操作是(填写代号)。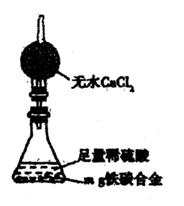
①用排水法测定H2的体积
②反应结束后,过滤、洗涤、干燥、称量残渣的质量
③测定反应前后装置和药品的总质量
根据下列流程处理废旧电路板来回收金属Cu,并制得高铁酸钾(K2 FeO4)。
据此回答问题: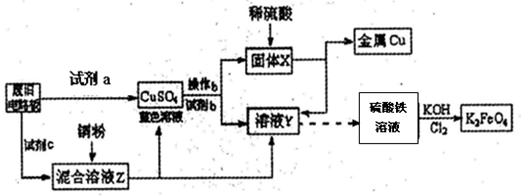
据此回答问题
(1)试剂a为试剂b为 (填写所选试剂代号)
| A.浓硫酸 | B.硫酸铁溶液 | C.氯水 | D.H2 O2和稀硫酸 E. Fe |
(2)加入过量试剂c,发生反应的离子方程式为__;溶液Z中金属离子可能有Cu2+、Fe2+、Fe3+,检验Fe3+的试剂为__ _ _(填化学式);欲测定溶液Z中Fe2+的浓度,需要用(填仪器名称)__ __配制一定浓度的KMnO4标准溶液。在滴定时KMnO4标准溶液应加入到(填“酸式”或“碱式”)滴定管中。
(3) K2FeO4是强氧化剂,与水发生反应:4FeO42-+10H2O="=" 4Fe(OH)3(胶体)+3O2↑+8OH-,产生11.2L(标况)O2时,转移电子的物质的量为。K2Fe04与FeCl3相比,净水效果更好的是_,理由是。
(4)高铁电池是一种新型可充电电池,总反应为:3Zn +2K2FeO4 +8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,电池工作时在正极放电的物质是:。
3Zn(OH)2+2Fe(OH)3+4KOH,电池工作时在正极放电的物质是:。
A、B、C、D、E是原子序数依次增大的短周期元素,A、D在周期表中的相对位置如表,且元素A的最高正化合价与最低负化合价的绝对值相差2,B与D属于同主族元素;元素C是一种银白色金属,放置在空气中会迅速变暗。
(1)D的原子结构示意图为;
(2)元素E在元素周期表中位于第族;
(3)C、D、E离子半径的大小关系为(用离子符号表示);
(4)元素B的单质与元素C的单质加热时生成化合物甲,化合物甲中所含化学键为
试写出甲与水反应的离子方程式;
(5)若乙是元素A的最简单气态氢化物,丙是元素C的最高价氧化物对应的水化物。
①pH相同的乙和丙的水溶液,分别用蒸馏水稀释到原来的x、y倍,稀释后两种溶液的pH仍然相同,则xy(填写“>”、“<”或“=” )
②在微电子工业中,乙的水溶液常用作刻蚀剂H2O2的清除剂,反应的产物不污染环境,其化学方程式为(不需要配平)。