高温下,某反应达平衡,平衡常数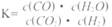 恒容时,温度升高,H2浓度减小。下列说法正确的是
恒容时,温度升高,H2浓度减小。下列说法正确的是
| A.该反应的焓变为正值 |
| B.恒温恒容下,增大压强,H2浓度一定减小 |
| C.升高温度,逆反应速率减小 |
D.该反应的化学方程式为CO+ H2O CO2+H2 CO2+H2 |
能将甲醇、乙醛、甲酸、乙酸四种液体物质鉴别出来的一种试剂(必要时可加热)是
| A.溴水 | B.新制的Cu(OH)2悬浊液 | C.银氨溶液 | D.FeCl3溶液 |
下列过程中,发生了消去反应的是
| A.C2H5Br和NaOH溶液混合共热 | B.一氯甲烷和苛性钾的乙醇溶液混合共热 |
| C.一溴丁烷与KOH的丁醇溶液混合共热 | D.氯苯与NaOH溶液混合共热 |
某烃的分子式为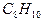 ,它不能使溴水褪色,但能使酸性高锰酸钾溶液褪色。该有机物苯环上的一氯代物只有2种,则该烃是
,它不能使溴水褪色,但能使酸性高锰酸钾溶液褪色。该有机物苯环上的一氯代物只有2种,则该烃是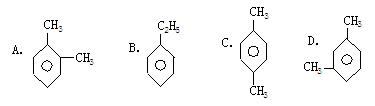
下列说法不正确的是
| A.同系物的化学性质相似 |
| B.同位素的化学性质几乎相同 |
| C.分子量相同的几种化合物互称为同分异构体 |
| D.同素异形体之间、同分异构体之间的转化属于物理变化 |
最近,媒体报道不法商贩销售“致癌大米”,已验证这种大米中含有黄曲霉毒素(AFTB),其分子结构式为如图所示,人体的特殊基因在黄曲霉素的作用下会发生突变,有转变为肝癌的可能。一般条件下跟1mol AFTB起反应的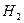 或NaOH的最大量分别是
或NaOH的最大量分别是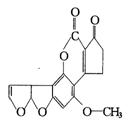
A.6mol;1mol B.5mol;1mol
C.6mol;2mol D.5mol;2mol